
12.1: Clases de materiales
- ID de página
- 21777
La unión en metales y semiconductores se puede describir utilizando la teoría de bandas, en la que se genera un conjunto de orbitales moleculares que se extienden por todo el sólido. El objetivo principal de aprendizaje de este módulo es describir las propiedades eléctricas de los sólidos utilizando la teoría de bandas.
Teoría de la banda
Para explicar las propiedades observadas de los metales, se necesita un enfoque más sofisticado que el modelo de mar de electrones comúnmente descrito. La teoría de los orbitales moleculares utilizada para explicar la unión deslocalizada π en iones poliatómicos y moléculas como NO 2 – , el ozono y el 1,3-butadieno se pueden adaptar para acomodar los niveles mucho más altos Número de orbitales atómicos que interactúan entre sí simultáneamente en los metales.
En una muestra de 1 mol de un metal, puede haber más de 10 24 interacciones orbitales a considerar. Sin embargo, en nuestra descripción orbital molecular de metales, comenzamos considerando un ejemplo unidimensional simple: una disposición lineal de n átomos de metal, cada uno de los cuales contiene un solo electrón en un orbital s. Usamos este ejemplo para describir un enfoque de enlace metálico llamado teoría de bandas, que supone que los orbitales de valencia de los átomos en un sólido interactúan, generando un conjunto de orbitales moleculares que se extienden por todo el sólido.
Sistemas unidimensionales
Si la distancia entre los átomos metálicos es lo suficientemente corta como para que los orbitales interactúen, producen orbitales moleculares de unión, antibondición y no unión. La parte izquierda de la Figura ( PageIndex {1} ) muestra el patrón de los orbitales moleculares que resulta de la interacción de los orbitales ns cuando n aumenta de 2 a 5.
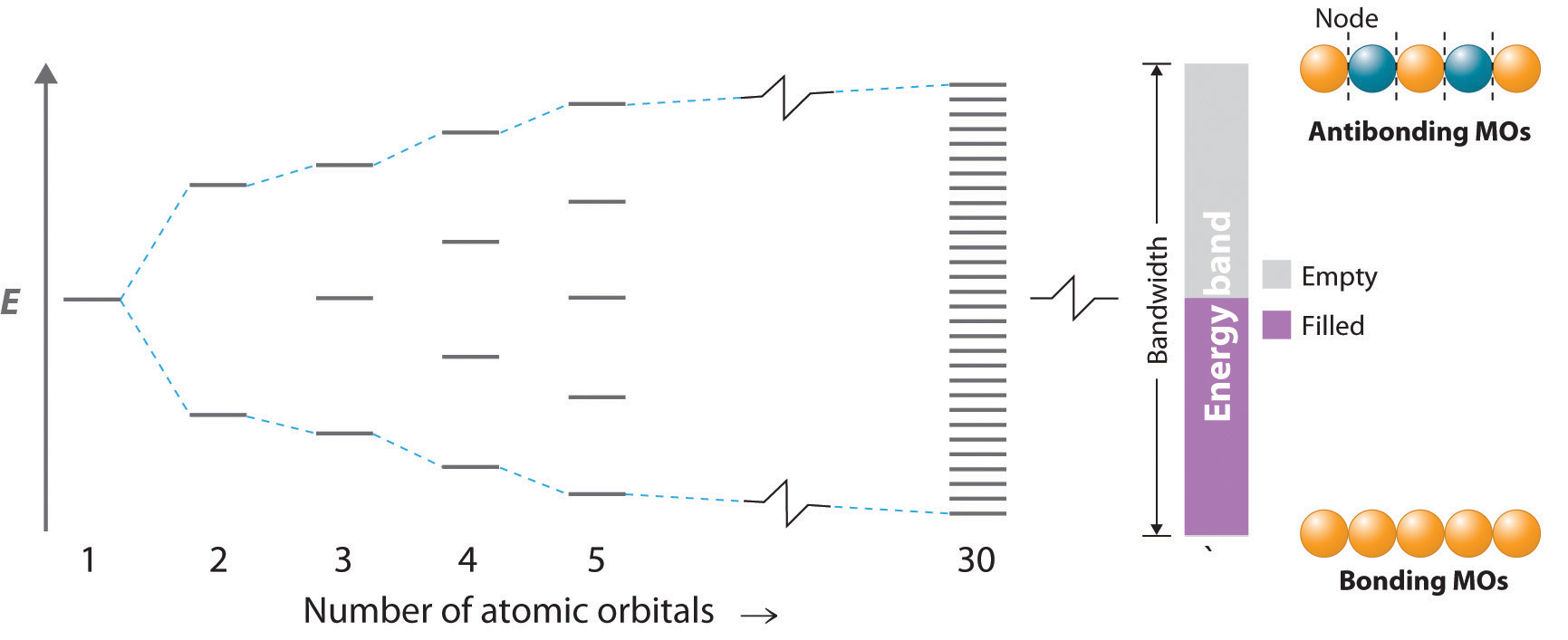
Como vimos anteriormente, el orbital de energía más baja es el orbital molecular que se une por completo, mientras que el orbital de energía más alta es el orbital molecular que se une por completo. Los orbitales moleculares de energía intermedia tienen menos ganglios que el orbital molecular totalmente antienvejecimiento. La separación de energía entre los orbitales adyacentes disminuye a medida que aumenta el número de orbitales que interactúan. Para n = 30, todavía hay niveles de energía discretos y bien resueltos, pero a medida que n aumenta de 30 a un número cercano al número de Avogadro, el espacio entre los niveles de energía adyacentes se vuelve casi infinitamente pequeño. El resultado es esencialmente un continuo de niveles de energía, como se muestra a la derecha en la Figura ( PageIndex {1} ), cada uno de los cuales corresponde a un orbital molecular particular que se extiende a lo largo de la matriz lineal de átomos metálicos. Los niveles que son más bajos en energía corresponden en su mayoría a combinaciones de unión de orbitales atómicos, los más altos en energía corresponden en su mayoría a combinaciones de antienvejecimiento, y aquellos en el medio corresponden a combinaciones esencialmente no unidas.
El conjunto continuo de niveles de energía permitidos que se muestra a la derecha en la Figura ( PageIndex {1} ) se denomina banda de energía. La diferencia de energía entre los niveles de energía más altos y más bajos es el ancho de banda y es proporcional a la fuerza de la interacción entre los orbitales en los átomos adyacentes: cuanto más fuerte es la interacción, mayor es el ancho de banda. Debido a que la banda contiene tantos niveles de energía como los orbitales moleculares, y el número de orbitales moleculares es el mismo que el número de orbitales atómicos que interactúan, la banda en la Figura ( PageIndex {1} ) contiene n niveles de energía correspondientes a la combinación de s orbitales de n átomos de metal. Cada uno de los orbitales originales puede contener un máximo de dos electrones, por lo que la banda puede acomodar un total de 2n electrones. Sin embargo, recuerde que cada uno de los átomos metálicos con los que comenzamos contenía solo un electrón en cada orbital, por lo que solo hay n electrones para colocar en la banda. Al igual que con los orbitales atómicos u orbitales moleculares, los electrones ocupan los niveles de energía más bajos disponibles. En consecuencia, solo se llena la mitad inferior de la banda. Esto corresponde al llenado de todos los orbitales moleculares de enlace en la matriz lineal de átomos de metal y da como resultado el enlace más fuerte posible.
Sistemas multidimensionales
El ejemplo anterior era una matriz unidimensional de átomos que solo tenían orbitales s. Extrapolar a sistemas bidimensionales o tridimensionales y átomos con electrones en los orbitales p y d es sencillo en principio, aunque en la práctica las matemáticas se vuelven más complejas y los orbitales moleculares resultantes son más difíciles de visualizar. Los diagramas de nivel de energía resultantes son esencialmente los mismos que el diagrama del ejemplo unidimensional en la Figura ( PageIndex {1} ), con la siguiente excepción: contienen tantas bandas como diferentes tipos de orbitales que interactúan. Debido a que diferentes orbitales atómicos interactúan de manera diferente, cada banda tendrá un ancho de banda diferente y se centrará en una energía diferente, correspondiente a la energía del orbital atómico original de un átomo aislado.
Brecha de banda
Debido a que los orbitales 1s, 2s y 2p de un átomo del período 3 están llenos de niveles centrales, no interactúan fuertemente con los orbitales correspondientes en los átomos adyacentes. Por lo tanto, forman bandas bastante estrechas que están bien separadas en energía (Figura ( PageIndex {2} )). Estas bandas están completamente llenas (tanto los niveles de unión como de antienvejecimiento están completamente poblados), por lo que no hacen una contribución neta a la unión en el sólido. La diferencia de energía entre el nivel más alto de una banda y el nivel más bajo de la siguiente es la brecha de banda. Representa un conjunto de energías prohibidas que no corresponden a ninguna combinación permitida de orbitales atómicos.
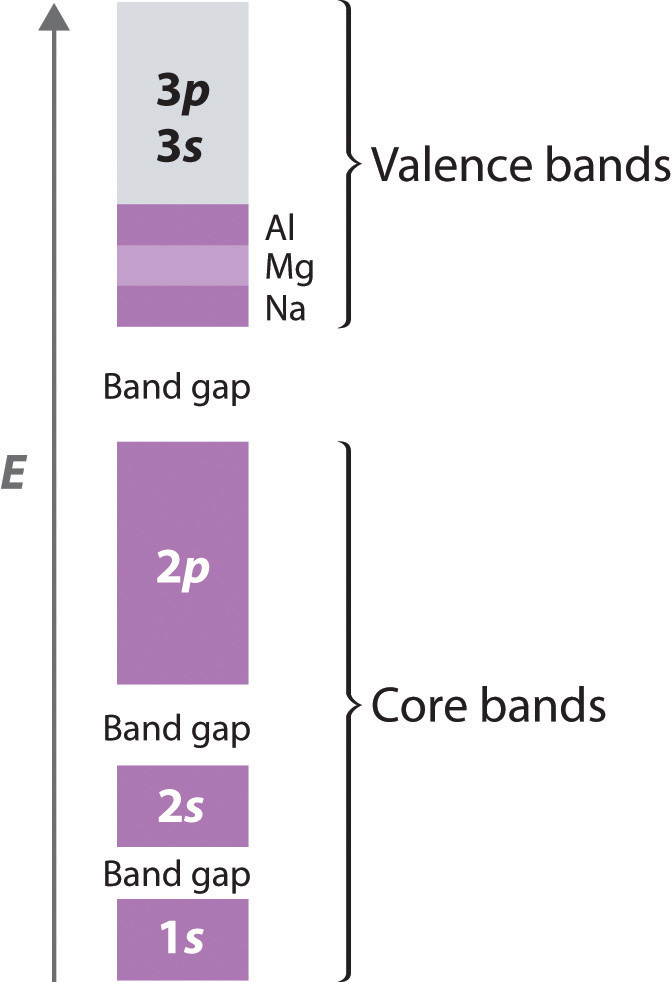
Debido a que se extienden más lejos del núcleo, los orbitales de valencia de los átomos adyacentes (3s y 3p en la Figura ( PageIndex {2} )) interactúan mucho más fuertemente entre sí que los niveles centrales llenos; Como resultado, las bandas de valencia tienen un ancho de banda mayor. De hecho, las bandas derivadas de los orbitales atómicos 3s y 3p son más anchas que la brecha de energía entre ellas, por lo que el resultado son bandas superpuestas. Estos tienen orbitales moleculares derivados de dos o más orbitales de valencia con energías similares. A medida que la banda de valencia se llena con uno, dos o tres electrones por átomo para Na, Mg y Al, respectivamente, la banda combinada que surge de la superposición de las bandas 3s y 3p también se está llenando; Tiene una capacidad total de ocho electrones por átomo (dos electrones por cada orbital 3s y seis electrones por cada conjunto de orbitales 3p). Con Na, por lo tanto, que tiene un electrón de valencia, la banda de valencia combinada se llena un octavo; con Mg (dos electrones de valencia), se llena un cuarto; y con Al, se llena tres octavos, como se indica en la Figura ( PageIndex {2} ). La banda de valencia parcialmente llena es absolutamente crucial para explicar el comportamiento metálico porque garantiza que hay niveles de energía desocupados en una energía infinitamente pequeña por encima del nivel ocupado más alto.
La teoría de bandas puede explicar virtualmente todas las propiedades de los metales. Los metales conducen electricidad, por ejemplo, porque solo se requiere una cantidad muy pequeña de energía para excitar un electrón de un nivel lleno a uno vacío, donde es libre de migrar rápidamente a través del cristal en respuesta a un campo eléctrico aplicado. Del mismo modo, los metales tienen altas capacidades de calor (como seguramente recordará de la última vez que un médico o una enfermera le colocaron un estetoscopio en la piel) porque los electrones en la banda de valencia pueden absorber la energía térmica al excitarse hacia la energía vacía baja. niveles. Finalmente, los metales son brillantes porque la luz de varias longitudes de onda puede ser absorbida, haciendo que los electrones de valencia se exciten en cualquiera de los niveles de energía vacía por encima del nivel ocupado más alto. Cuando los electrones se descomponen de nuevo a niveles bajos vacíos, emiten luz de diferentes longitudes de onda. Debido a que los electrones pueden excitarse desde muchos niveles de relleno diferentes en un sólido metálico y luego pueden descomponerse a cualquiera de los muchos niveles vacíos, la luz de diferentes longitudes de onda es absorbida y reemitida, lo que resulta en el aspecto brillante característico que asociamos con los metales.
Requisitos para el comportamiento metálico
Para que un sólido exhiba un comportamiento metálico,
- debe tener un conjunto de orbitales deslocalizados que formen una banda de niveles de energía permitidos, y
- la banda resultante debe estar parcialmente llena (10% –90%) con electrones.
Sin un conjunto de orbitales deslocalizados, no hay una vía por la cual los electrones puedan moverse a través del sólido.
La teoría de la banda explica la correlación entre la configuración electrónica de valencia de un metal y la fuerza de la unión metálica. Los electrones de valencia de los metales de transición ocupan sus orbitales de valencia ns, (n – 1) d y np (con una capacidad total de 18 electrones por átomo de metal) o sus orbitales ns y (n – 1) d (una capacidad total de 12 electrones por átomo de metal). Estos orbitales atómicos tienen una energía lo suficientemente cercana como para que las bandas derivadas se superpongan, por lo que los electrones de valencia no están confinados a un orbital específico. Los metales con electrones de valencia de 6 a 9 (que corresponden a los grupos 6–9) son los que tienen más probabilidades de llenar las bandas de valencia aproximadamente a la mitad. Esos electrones, por lo tanto, ocupan el mayor número posible de niveles de unión, mientras que el número de niveles de unión ocupados es mínimo. No es coincidencia que los elementos de estos grupos exhiban propiedades físicas consistentes con la presencia del enlace metálico más fuerte, como puntos de fusión muy altos.
Aisladores
A diferencia de los metales, los aislantes eléctricos son materiales que conducen la electricidad de manera deficiente porque sus bandas de valencia están llenas. La brecha de energía entre los niveles llenos más altos y los niveles vacíos más bajos es tan grande que los niveles vacíos son inaccesibles: la energía térmica no puede excitar un electrón de un nivel lleno a uno vacío. La estructura de banda de valencia del diamante, por ejemplo, se muestra en la Figura ( PageIndex {3a} ). Debido a que el diamante solo tiene 4 vecinos unidos en lugar de los 6 a 12 típicos de los metales, los orbitales de carbono 2s y 2p se combinan para formar dos bandas en el sólido, con una de menor energía que representa la unión de los orbitales moleculares y la de mayor energía que representa el antienvejecimiento orbitales moleculares. Cada banda puede acomodar cuatro electrones por átomo, por lo que solo la banda inferior está ocupada. Debido a que la brecha de energía entre la banda llena y la banda vacía es muy grande (530 kJ / mol), a temperaturas normales la energía térmica no puede excitar los electrones del nivel lleno en la banda vacía. Por lo tanto, no hay una vía por la cual los electrones puedan moverse a través del sólido, por lo que el diamante tiene una de las conductividades eléctricas más bajas conocidas.
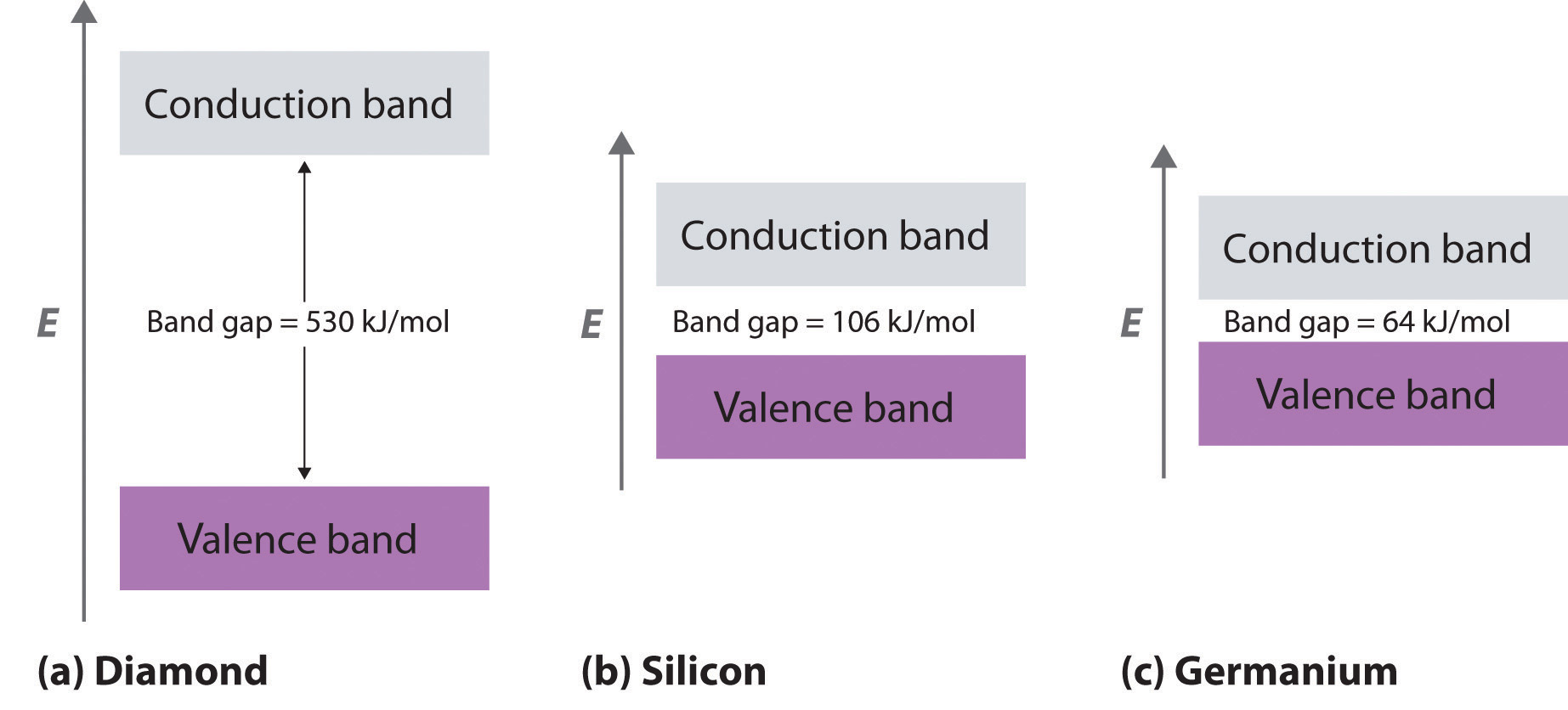
Semiconductores
¿Qué sucede si la diferencia de energía entre el nivel ocupado más alto y el nivel vacío más bajo es intermedia entre la de los conductores eléctricos y los aisladores? Este es el caso del silicio y el germanio, que tienen la misma estructura que el diamante. Debido a que los enlaces Si – Si y Ge – Ge son sustancialmente más débiles que los enlaces C – C, la brecha de energía entre las bandas llenas y vacías se vuelve mucho más pequeña a medida que bajamos el grupo 14 (parte (b) y parte (c) de la Figura ( PageIndex {2} )). En consecuencia, la energía térmica es capaz de excitar una pequeña cantidad de electrones de la banda de valencia llena de Si y Ge en la banda vacía por encima de ella, que se llama banda de conducción.
Los electrones excitantes de la banda de valencia llena a la banda de conducción vacía causan un aumento en la conductividad eléctrica por dos razones:
- Los electrones en la banda de conducción previamente vacante son libres de migrar a través del cristal en respuesta a un campo eléctrico aplicado.
- La excitación de un electrón de la banda de valencia produce un “agujero” en la banda de valencia que es equivalente a una carga positiva. El agujero en la banda de valencia puede migrar a través del cristal en la dirección opuesta a la del electrón en la banda de conducción por medio de un mecanismo de “brigada de cubeta” en el que un electrón adyacente llena el agujero, generando así un agujero donde el segundo electrón tenía estado, y así sucesivamente.
En consecuencia, Si es un conductor eléctrico mucho mejor que el diamante, y Ge es aún mejor, aunque ambos son conductores mucho más pobres que un metal típico (Figura ( PageIndex {4} )).

Las sustancias como el Si y Ge que tienen conductividades entre las de los metales y los aislantes se llaman semiconductores. Muchos compuestos binarios de los elementos del grupo principal exhiben un comportamiento semiconductor similar al de Si y Ge. Por ejemplo, el arseniuro de galio (GaAs) es isoelectrónico con Ge y tiene la misma estructura cristalina, con átomos alternos de Ga y As; No es sorprendente que también sea un semiconductor. La estructura electrónica de los semiconductores se compara con las estructuras de metales y aislantes en la Figura ( PageIndex {5} ).
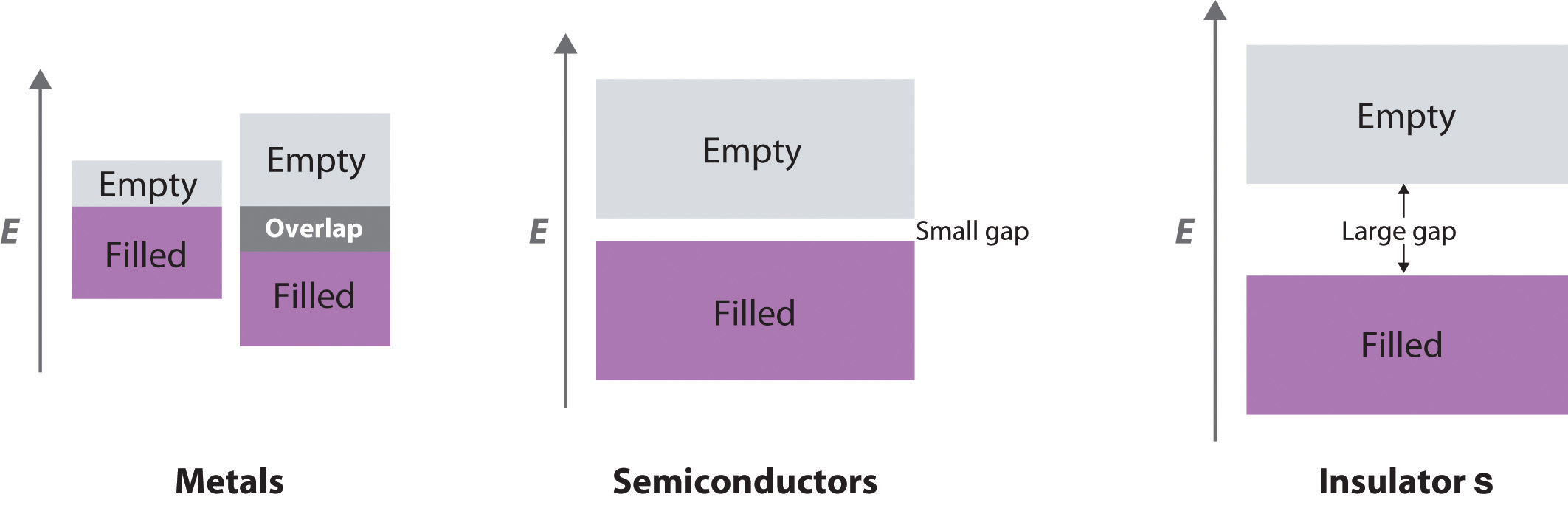
Temperatura y conductividad
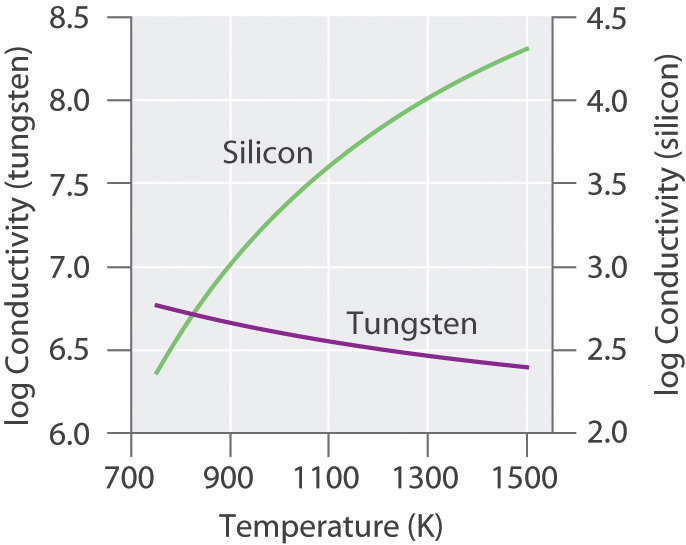
Debido a que la energía térmica puede excitar electrones a través del intervalo de banda en un semiconductor, el aumento de la temperatura aumenta el número de electrones que tienen suficiente energía cinética para ser promovidos a la banda de conducción. Por lo tanto, la conductividad eléctrica de un semiconductor aumenta rápidamente con el aumento de la temperatura, en contraste con el comportamiento de un cristal puramente metálico. En un metal, cuando un electrón viaja a través del cristal en respuesta a un potencial eléctrico aplicado, no puede viajar muy lejos antes de encontrarse y chocar con un núcleo metálico. Cuanto más a menudo ocurren tales encuentros, más lento es el movimiento neto del electrón a través del cristal y menor es la conductividad. A medida que aumenta la temperatura del sólido, los átomos metálicos en la red adquieren más y más energía cinética. Sin embargo, debido a que sus posiciones están fijas en la red, el aumento de la energía cinética aumenta solo la medida en que vibran alrededor de sus posiciones fijas. Por lo tanto, a temperaturas más altas, los núcleos metálicos chocan con los electrones móviles con mayor frecuencia y con mayor energía, disminuyendo así la conductividad. Sin embargo, este efecto es sustancialmente menor que el aumento de la conductividad con la temperatura exhibida por los semiconductores. Por ejemplo, la conductividad de un cable de tungsteno disminuye en un factor de solo aproximadamente dos en el rango de temperatura 750–1500 K, mientras que la conductividad del silicio aumenta aproximadamente 100 veces en el mismo rango de temperatura. Estas tendencias se ilustran en la Figura ( PageIndex {6} ).
Semiconductores de tipo n y p
El dopaje es un proceso utilizado para ajustar las propiedades eléctricas de los semiconductores comerciales mediante la introducción deliberada de pequeñas cantidades de impurezas. Si una impureza contiene más electrones de valencia que los átomos de la red del huésped (p. Ej., Cuando se introducen pequeñas cantidades de un átomo del grupo 15 en un cristal de un elemento del grupo 14), el sólido dopado tiene más electrones disponibles para conducir corriente que el puro anfitrión tiene. Como se muestra en la Figura ( PageIndex {7a} ), agregar una impureza como el fósforo a un cristal de silicio crea sitios ocasionales ricos en electrones en la red. La energía electrónica de estos sitios se encuentra entre los de la banda de valencia llena y la banda de conducción vacía, pero más cerca de la banda de conducción. Debido a que los átomos que se introdujeron están rodeados por átomos del huésped, y los electrones asociados con la impureza tienen una energía cercana a la banda de conducción, esos electrones adicionales se excitan relativamente fácilmente en la banda de conducción vacía del huésped. Dicha sustancia se llama semiconductor de tipo n, con n indicando que los portadores de carga añadidos son negativos (son electrones).
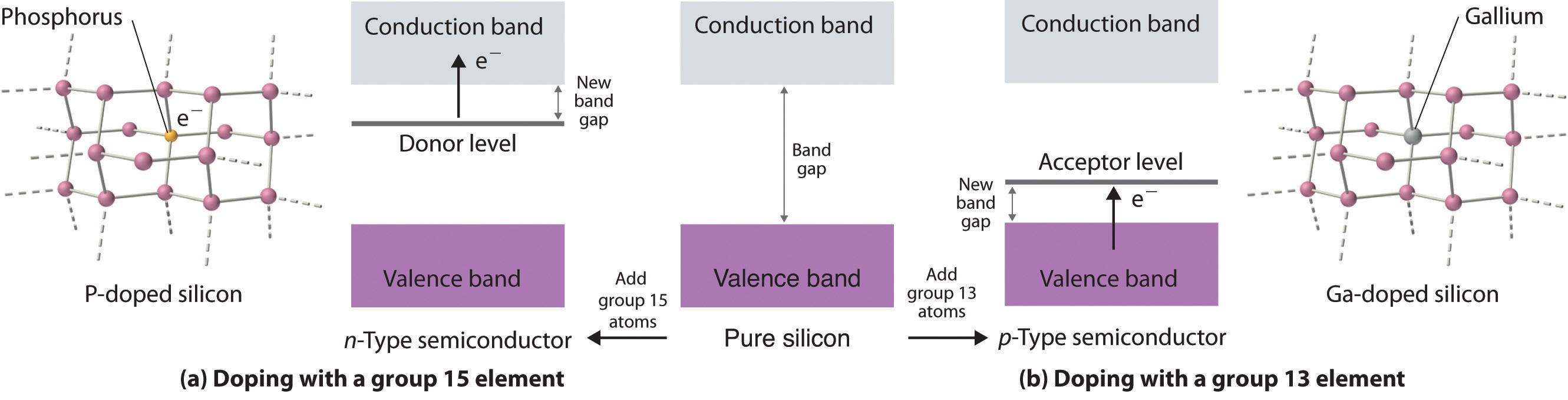
Si los átomos de impurezas contienen menos electrones de valencia que los átomos del huésped (p. Ej., Cuando se introducen pequeñas cantidades de un átomo del grupo 13 en un cristal de un elemento del grupo 14), el sólido dopado tiene menos electrones que el puro anfitrión. Quizás inesperadamente, esto también resulta en una mayor conductividad porque los átomos de impureza generan agujeros en la banda de valencia. Como se muestra en la Figura ( PageIndex {7b} ), agregar una impureza como el galio a un cristal de silicio crea sitios aislados deficientes en electrones en la red del huésped. La energía electrónica de estos sitios vacíos también se encuentra entre los de la banda de valencia llena y la banda de conducción vacía del huésped, pero mucho más cerca de la banda de valencia llena. Por lo tanto, es relativamente fácil excitar electrones de la banda de valencia del huésped a los átomos de impureza aislados, formando así agujeros en la banda de valencia. Este tipo de sustancia se llama semiconductor tipo p, con la p representando portador de carga positiva (es decir, un agujero). Los agujeros en lo que era una banda llena son tan efectivos como los electrones en una banda vacía para conducir electricidad.
La conductividad eléctrica de un semiconductor es aproximadamente proporcional al número de portadores de carga, por lo que el dopaje es una forma precisa de ajustar la conductividad de un semiconductor en un amplio rango. Toda la industria de semiconductores se basa en métodos para preparar muestras de Si, Ge o GaAs impregnadas con cantidades precisas de impurezas deseadas y ensamblar chips de silicio y otros dispositivos complejos con uniones entre semiconductores de tipo n y p en diferentes cantidades y disposiciones.
Debido a que el silicio no resiste bien las temperaturas superiores a aproximadamente 100 ° C, los científicos han estado interesados en desarrollar semiconductores hechos de diamantes, un material más estable térmicamente. Se ha desarrollado un nuevo método basado en la deposición de vapor, en el que una mezcla gaseosa se calienta a una temperatura alta para producir carbono que luego se condensa en un núcleo de diamante. Este es el mismo método que ahora se usa para crear diamantes cultivados, que no se pueden distinguir de los diamantes naturales. Los diamantes se calientan a más de 2000 ° C a alta presión para endurecerlos aún más. Dopando los diamantes con boro ha producido semiconductores de tipo p, mientras que dopando con boro y deuterio se logra un comportamiento de tipo n. Debido a su estabilidad térmica, los semiconductores de diamante tienen usos potenciales como microprocesadores en aplicaciones de alto voltaje.
Ejemplo ( PageIndex {1} )
Un sólido cristalino tiene la siguiente estructura de banda, con las áreas de color púrpura que representan las regiones ocupadas por electrones. La banda inferior está completamente ocupada por electrones, y el nivel superior está aproximadamente un tercio lleno de electrones.
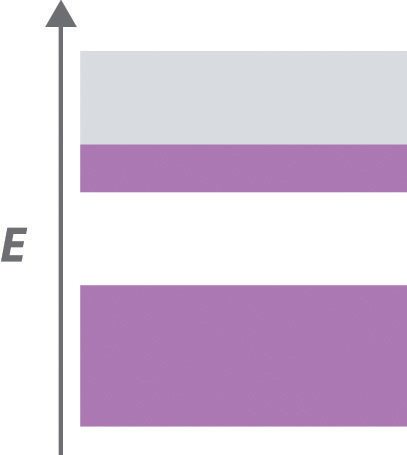
- Predecir las propiedades eléctricas de este sólido.
- ¿Qué pasaría con las propiedades eléctricas si se eliminaran todos los electrones de la banda superior? ¿Usaría un oxidante o reductor químico para efectuar este cambio?
- ¿Qué pasaría con las propiedades eléctricas si se agregaran suficientes electrones para llenar completamente la banda superior? ¿Usaría un oxidante o reductor químico para efectuar este cambio?
Dado : estructura de banda
Preguntado por : variaciones en las propiedades eléctricas con condiciones
Estrategia :
- B basado en la ocupación de las bandas inferior y superior, predicen si la sustancia será un conductor eléctrico. Luego predice cómo cambiará su conductividad con la temperatura.
- Después de que todos los electrones se eliminan de la banda superior, predice cómo la brecha de banda afectaría las propiedades eléctricas del material. Determine si usaría un oxidante o reductor químico para eliminar los electrones de la banda superior.
- Predecir el efecto de una banda superior llena sobre las propiedades eléctricas del sólido. Luego decida si usaría un oxidante o un reductor para llenar la banda superior.
Solución :
- El material tiene una banda parcialmente llena, que es crítica para el comportamiento metálico. Por lo tanto, el sólido se comportará como un metal, con una alta conductividad eléctrica que disminuye ligeramente con el aumento de la temperatura.
- La eliminación de todos los electrones de la banda superior parcialmente llena crearía un sólido con una banda inferior llena y una banda superior vacía, separadas por una brecha de energía. Si el espacio entre bandas es grande, el material será un aislante eléctrico. Si el espacio es relativamente pequeño, la sustancia será un semiconductor cuya conductividad eléctrica aumenta rápidamente al aumentar la temperatura. Eliminar los electrones requeriría un oxidante porque los oxidantes aceptan electrones.
- Agregar suficientes electrones para llenar completamente la banda superior produciría un aislante eléctrico. Sin otra banda vacía relativamente cercana en energía por encima de la banda llena, el comportamiento de los semiconductores sería imposible. Agregar electrones al sólido requeriría un reductor porque los reductores son donantes de electrones.
Ejercicio ( PageIndex {1} )
Una sustancia tiene la siguiente estructura de banda, en la que la banda inferior está medio llena de electrones (área púrpura) y la banda superior está vacía.
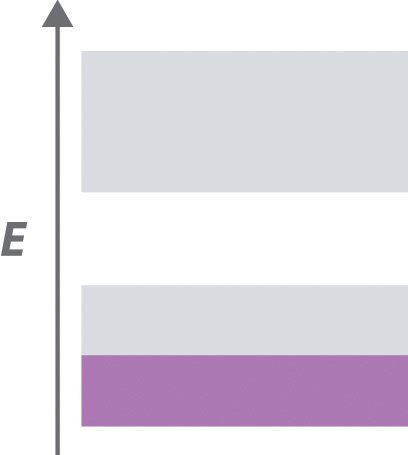
- Predice las propiedades eléctricas del sólido.
- ¿Qué pasaría con las propiedades eléctricas si se eliminaran todos los electrones de la banda inferior? ¿Usaría un oxidante o reductor químico para efectuar este cambio?
- ¿Qué pasaría con las propiedades eléctricas si se agregaran suficientes electrones para llenar completamente la banda inferior? ¿Usaría un oxidante o reductor químico para efectuar este cambio?
Respuesta :
- El sólido tiene una banda parcialmente llena, por lo que tiene las propiedades eléctricas de un conductor.
- Eliminar todos los electrones de la banda inferior produciría un aislante eléctrico con dos bandas vacías. Se requiere un oxidante.
- Agregar suficientes electrones para llenar completamente el nivel inferior daría como resultado un aislante eléctrico si la brecha de energía entre las bandas superior e inferior es relativamente grande, o un semiconductor si la brecha de banda es relativamente pequeña. Se requiere un reductor.
- El comportamiento metálico requiere un conjunto de orbitales deslocalizados y una banda de niveles de energía permitidos que está parcialmente ocupada.
- La conductividad eléctrica de un semiconductor aumenta al aumentar la temperatura, mientras que la conductividad eléctrica de un metal disminuye al aumentar la temperatura.
- Los semiconductores de tipo n son portadores de carga negativa; La impureza tiene más electrones de valencia que el huésped. Los semiconductores de tipo p son portadores de carga positiva; La impureza tiene menos electrones de valencia que el huésped.
Resumen
La teoría de la banda supone que los orbitales de valencia de los átomos en un sólido interactúan para generar un conjunto de orbitales moleculares que se extienden por todo el sólido; El conjunto continuo de niveles de energía permitidos es una banda de energía. La diferencia de energía entre los niveles más altos y más bajos permitidos dentro de una banda dada es el ancho de banda, y la diferencia de energía entre el nivel más alto de una banda y el nivel más bajo de la banda por encima es el intervalo de banda. Si el ancho de las bandas adyacentes es mayor que la brecha de energía entre ellas, se producen bandas superpuestas, en las cuales los orbitales moleculares derivados de dos o más tipos de orbitales de valencia tienen energías similares. Las propiedades metálicas dependen de una banda parcialmente ocupada que corresponde a un conjunto de orbitales moleculares que se extienden por todo el sólido para formar una banda de niveles de energía. Si un sólido tiene una banda de valencia llena con una banda vacía relativamente baja (una banda de conducción), entonces los electrones pueden ser excitados por la energía térmica de la banda llena a la banda vacía, donde pueden migrar a través del cristal, lo que resulta en conductividad eléctrica. Los aisladores eléctricos son malos conductores porque sus bandas de valencia están llenas. Los semiconductores tienen conductividades eléctricas intermedias entre las de aisladores y metales. La conductividad eléctrica de los semiconductores aumenta rápidamente al aumentar la temperatura, mientras que la conductividad eléctrica de los metales disminuye lentamente al aumentar la temperatura. Las propiedades de los semiconductores pueden modificarse mediante dopaje o la introducción de impurezas. Agregar un elemento con más electrones de valencia que los átomos del huésped puebla la banda de conducción, lo que resulta en un semiconductor de tipo n con conductividad eléctrica aumentada. Agregar un elemento con menos electrones de valencia que los átomos del huésped genera agujeros en la banda de valencia, lo que resulta en un semiconductor de tipo p que también exhibe una mayor conductividad eléctrica.