Los factores que afectan la velocidad de reacción de una reacción química, que pueden determinar si se forma un producto deseado. En esta sección, le mostraremos cómo determinar cuantitativamente la velocidad de reacción.
Leyes de tarifas
Típicamente, las velocidades de reacción disminuyen con el tiempo porque las concentraciones de reactivo disminuyen a medida que los reactivos se convierten en productos. Las velocidades de reacción generalmente aumentan cuando se incrementan las concentraciones de reactivo. Esta sección examina las expresiones matemáticas llamadas leyes de velocidad , que describen las relaciones entre las tasas de reactivos y las concentraciones de reactivos. Las leyes de tarifas son descripciones matemáticas de datos verificables experimentalmente.
Las leyes de tarifas pueden redactarse desde dos perspectivas diferentes pero relacionadas. Una ley de velocidad diferencial expresa la velocidad de reacción en términos de cambios en la concentración de uno o más reactivos (Δ [R]) durante un intervalo de tiempo específico (Δt). Por el contrario, una ley de velocidad integrada describe la velocidad de reacción en términos de la concentración inicial ([R] 0 ) y la concentración medida de uno o más reactivos ([R]) después una cantidad de tiempo dada (t); Las leyes de tasas integradas se analizan con más detalle más adelante . La ley de tasa integrada se deriva utilizando el cálculo para integrar la ley de tasa diferencial. Ya sea que use una ley de velocidad diferencial o una ley de velocidad integrada, asegúrese siempre de que la ley de velocidad proporcione las unidades adecuadas para la velocidad de reacción, generalmente moles por litro por segundo (M / s).
Órdenes de reacción
Para una reacción con la ecuación general:
[aA + bB rightarrow cC + dD label {14.3.1} ]
la ley de tasas determinada experimentalmente generalmente tiene la siguiente forma:
[ text {rate} = k [A] ^ m [B] ^ n label {14.3.2} ]
La constante de proporcionalidad ( k ) se denomina constante de velocidad , y su valor es característico de la reacción y las condiciones de reacción. Una reacción dada tiene un valor constante de velocidad particular bajo un conjunto dado de condiciones, tales como temperatura, presión y solvente; variar la temperatura o el solvente usualmente cambia el valor de la constante de velocidad. Sin embargo, el valor numérico de k no cambia a medida que la reacción progresa bajo un conjunto dado de condiciones.
Bajo un conjunto dado de condiciones, el valor de la constante de velocidad no cambia a medida que avanza la reacción.
La velocidad de reacción depende de la constante de velocidad para el conjunto dado de condiciones de reacción y la concentración de A y B elevada a las potencias m y n , respectivamente. Los valores de m y n se derivan de mediciones experimentales de los cambios en las concentraciones de reactivo a lo largo del tiempo e indican el orden de reacción , el grado en que la velocidad de reacción depende de la concentración de cada reactivo; m y n no necesitan ser enteros. Por ejemplo, La ecuación ( ref {14.3.2} ) nos dice que La ecuación ( ref {14.3.1} ) es m orden en el reactivo A y n orden en el reactivo B. Es importante recordar que n y m [ 19459016] no están relacionados con los coeficientes estequiométricos a y b en la ecuación química equilibrada y deben determinarse experimentalmente . El orden de reacción general es la suma de todos los exponentes en la ley de velocidad: m + n .
Los órdenes de las reacciones (p. Ej. N y m) no están relacionados con los coeficientes estequiométricos en el químico equilibrado (p. Ej., a y b).
Para ilustrar cómo los químicos interpretan una ley de tasa diferencial, considere la ley de tasa derivada experimentalmente para la hidrólisis de t -bromuro de bromuro en acetona acuosa al 70%.
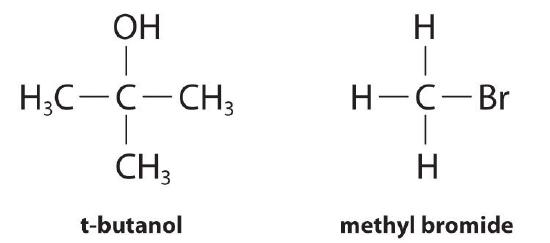
Esta reacción produce t -butanol de acuerdo con la siguiente ecuación:
[(CH_3) _3CBr _ {(soln)} + H_2O _ {(soln)} rightarrow (CH_3) _3COH _ {(soln)} + HBr _ {(soln)} label {14.3.3} ] [19459001 ]
Combinando la expresión de velocidad en la ecuación ( ref {14.3.2} ) con la definición de velocidad de reacción promedio
[ textrm {tasa} = – dfrac { Delta [ textrm A]} { Delta t} ]
da una expresión general para la ley de tasa diferencial:
[ textrm {rate} = – dfrac { Delta [ textrm A]} { Delta t} = k [ textrm A] ^ m [ textrm B] ^ n label {14.3.4 } ]
Al insertar las identidades de los reactivos en la Ecuación ( ref {14.3.4} ) se obtiene la siguiente expresión para la ley de velocidad diferencial para la reacción:
[ textrm {rate} = – dfrac { Delta [ mathrm {(CH_3) _3CBr}]} { Delta t} = k [ mathrm {(CH_3) _3CBr}] ^ m [ mathrm {H_2O}] ^ n label {14.3.5} ]
Los experimentos para determinar la ley de velocidad para la hidrólisis de t -bromuro de butilo muestran que la velocidad de reacción es directamente proporcional a la concentración de (CH 3 ) 3 [ 19459009] CBr pero es independiente de la concentración de agua. Por lo tanto, myn en la ecuación ( ref {14.3.4} ) son 1 y 0, respectivamente, y,
[ text {rate} = k [(CH_3) _3CBr] ^ 1 [H_2O] ^ 0 = k [(CH_3) _3CBr] label {14.3.6} ]
Debido a que el exponente para el reactivo es 1, la reacción es de primer orden en (CH 3 ) 3 CBr. Es el orden cero en el agua porque el exponente para [H 2 O] es 0. (Recuerde que cualquier cosa elevada a la potencia cero es igual a 1.) Por lo tanto, el orden general de reacción es 1 + 0 = 1. Las órdenes de reacción establecen en términos prácticos que duplicar la concentración de (CH 3 ) 3 CBr duplica la velocidad de reacción de la reacción de hidrólisis, reduciendo a la mitad la concentración de (CH 3 [ 19459009]) 3 CBr reduce a la mitad la velocidad de reacción, y así sucesivamente. Por el contrario, aumentar o disminuir la concentración de agua no tiene ningún efecto sobre la velocidad de reacción. (Nuevamente, cuando se trabaja con leyes de velocidad, no existe una correlación simple entre la estequiometría de la reacción y la ley de velocidad. Los valores de k , m y n [ 19459016] en la ley de velocidad debe determinarse experimentalmente.) Los datos experimentales muestran que k tiene el valor 5,15 × 10 −4 s −1 a 25 ° C . La constante de velocidad tiene unidades de segundos recíprocos (s −1 ) porque la velocidad de reacción se define en unidades de concentración por unidad de tiempo (M / s). Las unidades de una constante de velocidad dependen de la ley de velocidad para una reacción particular.
En condiciones idénticas a las de la reacción t -butilbromuro, la ley de velocidad diferencial derivada experimentalmente para la hidrólisis del metilbromuro (CH 3 Br) es la siguiente: [ 19459001]
[ textrm {rate} = – dfrac { Delta [ mathrm {CH_3Br}]} { Delta t} = k ‘[ mathrm {CH_3Br}] label {14.3.7} ] [ 19459001]
Esta reacción también tiene un orden de reacción global de 1, pero la constante de velocidad en Ecuación ( ref {14.3.7} ) es aproximadamente 10 6 veces menor que eso para t -bromuro de butilo. Por lo tanto, el bromuro de metilo se hidroliza aproximadamente 1 millón de veces más lentamente que el bromuro de t -butilo, y esta información le dice a los químicos cómo difieren las reacciones a nivel molecular.
Con frecuencia, los cambios en las condiciones de reacción también producen cambios en una ley de velocidad. De hecho, los químicos a menudo alteran las condiciones de reacción para estudiar la mecánica de una reacción. Por ejemplo, cuando t -bromuro de butilo se hidroliza en una solución acuosa de acetona que contiene iones OH – en lugar de solo en acetona acuosa, la ley de velocidad diferencial para la reacción de hidrólisis no cambia. En contraste, para el bromuro de metilo, la ley de tasa diferencial se convierte en
[ text {rate} = k ″ [CH_3Br] [OH ^ -] ]
con un orden de reacción global de 2. Aunque las dos reacciones proceden de manera similar en solución neutral, proceden de manera muy diferente en presencia de una base, proporcionando pistas sobre cómo difieren las reacciones a nivel molecular.
se ha determinado experimentalmente que es (tasa = k [NO] ^ 2 [H_2] ). ¿Cuáles son los órdenes con respecto a cada reactivo y cuál es el orden general de la reacción?
- Respuesta
-
- orden en NO = 2
- orden en H 2 = 1
- orden general = 3
La ley de velocidad para la reacción entre metanol y acetato de etilo se determina, bajo ciertas condiciones, experimentalmente:
[ ce {velocidad} = k [ ce {CH3OH}] ]
¿Cuál es el orden de reacción con respecto al metanol y el acetato de etilo, y cuál es el orden general de reacción?
- Respuesta
-
- orden en CH 3 OH = 1
- orden en CH 3 CH 2 OCOCH 3 = 0
- orden general = 1
Determinación de la ley de velocidad de una reacción
El número de mecanismos fundamentalmente diferentes (conjuntos de pasos en una reacción) es en realidad bastante pequeño en comparación con el gran número de reacciones químicas que pueden ocurrir. Por lo tanto, comprender los mecanismos de reacción puede simplificar lo que podría parecer una variedad confusa de reacciones químicas. El primer paso para descubrir el mecanismo de reacción es determinar la ley de velocidad de reacción. Esto se puede hacer diseñando experimentos que midan la (s) concentración (es) de uno o más reactivos o productos en función del tiempo. Para la reacción (productos A + B rightarrow ), por ejemplo, necesitamos determinar k y los exponentes m y n en la siguiente ecuación :
[ text {rate} = k [A] ^ m [B] ^ n label {14.4.11} ]
Para hacer esto, podríamos mantener constante la concentración inicial de B mientras variamos la concentración inicial de A y calculamos la velocidad de reacción inicial. Esta información nos permitiría deducir el orden de reacción con respecto a A. De manera similar, podríamos determinar el orden de reacción con respecto a B al estudiar la velocidad de reacción inicial cuando la concentración inicial de A se mantiene constante mientras que la concentración inicial de B varía . En ejemplos anteriores, determinamos el orden de reacción con respecto a un reactivo dado comparando las diferentes velocidades obtenidas cuando solo se cambió la concentración del reactivo en cuestión. Una forma alternativa de determinar los órdenes de reacción es establecer una proporción utilizando las leyes de velocidad para dos experimentos diferentes. Los datos de velocidad para una reacción hipotética del tipo (A + B productos de la derecha ) se dan en Tabla ( PageIndex {1} ) .
| Experimento | [A] (M) | [B] (M) | Velocidad inicial (M / min) |
|---|---|---|---|
| 1 | 0,50 | 0,50 | 8,5 × 10 −3 |
| 2 | 0,75 | 0,50 | 19 × 10 −3 |
| 3 | 1,00 | 0,50 | 34 × 10 −3 |
| 4 | 0,50 | 0,75 | 8,5 × 10 −3 |
| 5 | 0,50 | 1,00 | 8,5 × 10 −3 |
La ley de velocidad general para la reacción se da en Ecuación ( ref {14.4.11} ) . Podemos obtener m o n directamente usando una proporción de las leyes de velocidad para dos experimentos en los que la concentración de un reactivo es la misma, como los Experimentos 1 y 3 en [19459010 ] Tabla ( PageIndex {3} ) .
[ dfrac { mathrm {rate_1}} { mathrm {rate_3}} = dfrac {k [ textrm A_1] ^ m [ textrm B_1] ^ n} {k [ textrm A_3] ^ m [ textrm B_3] ^ n} ]
Insertar los valores apropiados de Tabla ( PageIndex {3} ) ,
[ dfrac {8.5 times10 ^ {- 3} textrm {M / min}} {34 times10 ^ {- 3} textrm {M / min}} = dfrac {k [ textrm { 0.50 M}] ^ m [ textrm {0.50 M}] ^ n} {k [ textrm {1.00 M}] ^ m [ textrm {0.50 M}] ^ n} ]
Debido a que 1.00 a cualquier potencia es 1, [1.00 M] m = 1.00 M. Podemos cancelar términos similares para dar 0.25 = [0.50] m , que también se puede escribir como 1/4 = [1/2] m . Por lo tanto, podemos concluir que m = 2 y que la reacción es de segundo orden en A. Al seleccionar dos experimentos en los que la concentración de B es la misma, pudimos resolver m [19459016 ]
Por el contrario, al seleccionar dos experimentos en los que la concentración de A es la misma (por ejemplo, los experimentos 5 y 1), podemos resolver n .
( dfrac { mathrm {rate_1}} { mathrm {rate_5}} = dfrac {k [ mathrm {A_1}] ^ m [ mathrm {B_1}] ^ n} {k [ mathrm {A_5}] ^ m [ mathrm {B_5}] ^ n} )
Sustituyendo los valores apropiados de Tabla ( PageIndex {3} ) ,
[ dfrac {8.5 times10 ^ {- 3} textrm {M / min}} {8.5 times10 ^ {- 3} textrm {M / min}} = dfrac {k [ textrm { 0.50 M}] ^ m [ textrm {0.50 M}] ^ n} {k [ textrm {0.50 M}] ^ m [ textrm {1.00 M}] ^ n} ]
Cancelando hojas 1.0 = [0.50] n , que da (n = 0 ); es decir, la reacción es de orden cero en (B ). La ley de tasas determinada experimentalmente es, por lo tanto,
tasa = k [A] 2 [B] 0 = k [A] 2
Ahora podemos calcular la constante de velocidad insertando los datos de cualquier fila de Tabla ( PageIndex {3} ) en la ley de velocidad determinada experimentalmente y resolviendo para (k ). Usando el Experimento 2, obtenemos
19 × 10 −3 M / min = k (0,75 M) 2
3,4 × 10 −2 M −1 · min −1 = k
Debe verificar que el uso de datos de cualquier otra fila de la Tabla ( PageIndex {1} ) proporcione la misma tasa constante. Esto debe ser cierto siempre que las condiciones experimentales, como la temperatura y el disolvente, sean las mismas.
Resumen
La ley de velocidad para una reacción es una relación matemática entre la velocidad de reacción y las concentraciones de especies en solución. Las leyes de velocidad pueden expresarse como una ley de velocidad diferencial, que describe el cambio en las concentraciones de reactivo o producto en función del tiempo, o como una ley de velocidad integrada, que describe las concentraciones reales de reactivos o productos en función del tiempo. La constante de velocidad ( k ) de una ley de velocidad es una constante de proporcionalidad entre la velocidad de reacción y la concentración de reactivo. El exponente al que se eleva una concentración en una ley de velocidad indica el orden de reacción, el grado en que la velocidad de reacción depende de la concentración de un reactivo particular.