El modelo de mecánica cuántica nos permitió determinar las energías de los orbitales atómicos de hidrógeno; ahora nos gustaría extender esto para describir la estructura electrónica de cada elemento en la Tabla Periódica. El proceso de describir la estructura electrónica de cada átomo consiste, esencialmente, en comenzar con hidrógeno y agregar un protón y un electrón a la vez para crear el siguiente elemento más pesado en la tabla; sin embargo, las interacciones entre electrones hacen que este proceso sea un poco más complicado de lo que parece. Todos los núcleos estables que no sean hidrógeno también contienen uno o más neutrones. Sin embargo, debido a que los neutrones no tienen carga eléctrica, pueden ignorarse en la siguiente discusión. Sin embargo, antes de demostrar cómo hacer esto, debemos introducir el concepto de espín electrónico y el principio de Pauli.
Orbitales y sus energías
A diferencia de los átomos similares al hidrógeno con un solo electrón, en los átomos multielectrónicos los valores de los números cuánticos n y l determinan las energías de un orbital. Las energías de los diferentes orbitales para un átomo multielectrónico típico se muestran en la Figura ( PageIndex {1} ). Dentro de una capa principal dada de un átomo multielectrónico, las energías orbitales aumentan con el aumento l . Un orbital ns siempre se encuentra debajo del orbital np correspondiente, que a su vez se encuentra debajo del orbital nd .
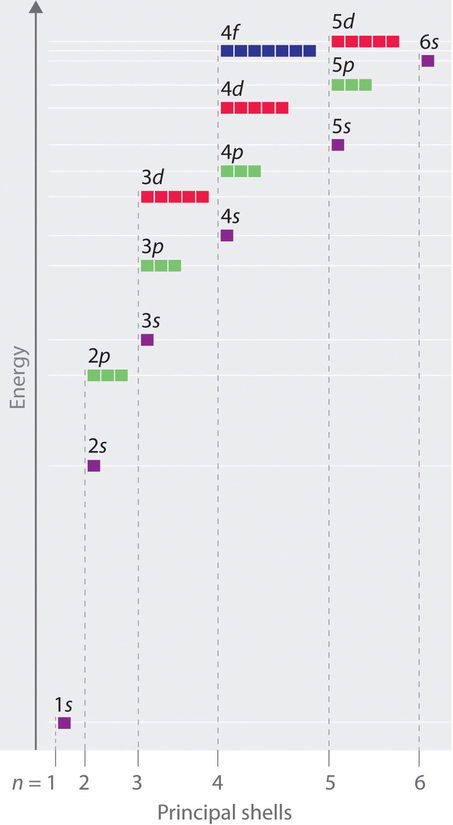
Estas diferencias de energía son causadas por los efectos de blindaje y penetración , la medida en que un orbital dado se encuentra dentro de otros orbitales llenos. Por ejemplo, un electrón en el orbital 2 s penetra dentro de un orbital 1 s lleno más que un electrón en un orbital 2 p . Como los electrones, todos cargados negativamente, se repelen entre sí, un electrón más cercano al núcleo protege parcialmente a un electrón más alejado del núcleo del efecto atractivo del núcleo cargado positivamente. Por lo tanto, en un átomo con un orbital lleno de s , la carga nuclear efectiva ( Z eff ) experimentado por un 2 s El electrón es mayor que el Z eff experimentado por un electrón 2 p . En consecuencia, el electrón 2 s está más estrechamente unido al núcleo y tiene una energía más baja, consistente con el orden de energías mostrado en la Figura ( PageIndex {1} ).
Debido al blindaje de electrones, (Z_ {eff} ) aumenta más rápidamente en una fila de la tabla periódica que en una columna.
Observe en la Figura ( PageIndex {1} ) que la diferencia en las energías entre subcapas puede ser tan grande que las energías de los orbitales de diferentes capas principales pueden llegar a ser aproximadamente iguales. Por ejemplo, la energía de los 3 d orbitales en la mayoría de los átomos es en realidad entre las energías de los 4 s y los 4 p orbitales
Giro electrónico: el cuarto número cuántico
Cuando los científicos analizaron los espectros de emisión y absorción de los elementos más de cerca, vieron que para los elementos que tienen más de un electrón, casi todas las líneas en los espectros eran en realidad pares de líneas muy cercanas. Debido a que cada línea representa un nivel de energía disponible para los electrones en el átomo, hay el doble de niveles de energía disponibles que se predecirían únicamente en función de los números cuánticos (n ), (l ) y (m_l ) . Los científicos también descubrieron que la aplicación de un campo magnético hacía que las líneas en los pares se separaran más. En 1925, dos estudiantes de posgrado en física en los Países Bajos, George Uhlenbeck (1900–1988) y Samuel Goudsmit (1902–1978), propusieron que las divisiones fueron causadas por un electrón que gira sobre su eje, al igual que la Tierra gira sobre su eje. Cuando un objeto con carga eléctrica gira, produce un momento magnético paralelo al eje de rotación, haciendo que se comporte como un imán. Aunque el electrón no puede verse únicamente como una partícula, girando o no, es indiscutible que tiene un momento magnético. Este momento magnético se llama espín electrónico .
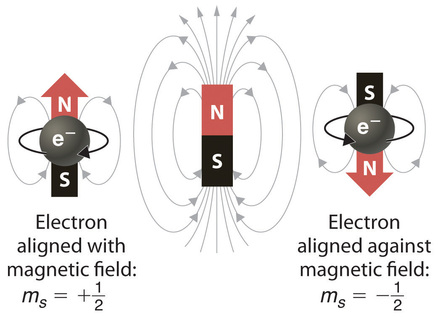
En un campo magnético externo, el electrón tiene dos orientaciones posibles (Figura Figura ( PageIndex {2} )). Estos se describen mediante un cuarto número cuántico ( m s ), que para cualquier electrón puede tener solo dos valores posibles, designados + ½ (arriba) y – ½ (abajo) para indicar que las dos orientaciones son opuestas; el subíndice s es para spin. Un electrón se comporta como un imán que tiene una de dos orientaciones posibles, alineadas con el campo magnético o contra él.
El principio de exclusión de Pauli
Las implicaciones del espín electrónico para la química fueron reconocidas casi de inmediato por un físico austriaco, Wolfgang Pauli (1900-1958; Premio Nobel de Física, 1945), quien determinó que cada orbital no puede contener más de dos electrones. Desarrolló el principio de exclusión de Pauli : No hay dos electrones en un átomo que puedan tener los mismos valores de los cuatro números cuánticos (n, l, m l ] , m s ).
Al dar los valores de n , l y m l , también especificamos un orbital particular (p. ej., 1 s con n = 1, l = 0, m l ] = 0). Porque m s tiene solo dos valores posibles (+ ½ o −½), dos electrones, y solo dos electrones , pueden ocupar cualquier orbital dado, uno con giro hacia arriba y otro con giro hacia abajo. Con esta información, podemos proceder a construir la tabla periódica completa, que originalmente se basó en las propiedades físicas y químicas de los elementos conocidos.
Resumen
La disposición de los átomos en la tabla periódica surge de la disposición de energía más baja de los electrones en la capa de valencia. Además de los tres números cuánticos ( n , l , m l ) dictados por la mecánica cuántica, Se requiere un cuarto número cuántico para explicar ciertas propiedades de los átomos. Este es el número cuántico de espín electrónico ( m s ), que puede tener valores de + ½ o −½ para cualquier electrón, correspondiente a las dos orientaciones posibles de un electrón en un campo magnético. El concepto de espín electrónico tiene importantes consecuencias para la química porque el principio de exclusión de Pauli implica que ningún orbital puede contener más de dos electrones (con espín opuesto).