Al igual que con los compuestos iónicos, el sistema para nombrar compuestos covalentes permite a los químicos escribir la fórmula molecular a partir del nombre y viceversa. Esta y la siguiente sección describen las reglas para nombrar compuestos covalentes simples, comenzando con compuestos inorgánicos y luego convirtiéndose en compuestos orgánicos simples que contienen solo carbono e hidrógeno.
Cuando los químicos sintetizan un nuevo compuesto, es posible que aún no conozcan su fórmula molecular o estructural. En tales casos, generalmente comienzan por determinar su fórmula empírica, el número relativo de átomos de los elementos en un compuesto, reducido a los números enteros más pequeños. Debido a que la fórmula empírica se basa en mediciones experimentales de los números de átomos en una muestra del compuesto, solo muestra las proporciones de los números de los elementos presentes. La diferencia entre las fórmulas empíricas y moleculares se puede ilustrar con butano, un compuesto covalente utilizado como combustible en encendedores desechables. La fórmula molecular para el butano es ( ce {C4H10} ). La relación de átomos de carbono a átomos de hidrógeno en butano es 4:10, que se puede reducir a 2: 5. La fórmula empírica para el butano es por lo tanto ( ce {C2H5} ). La unidad de fórmula es la agrupación absoluta de átomos o iones representados por la fórmula empírica de un compuesto, iónico o covalente. El butano tiene la fórmula empírica ( ce {C2H5} ), pero contiene dos unidades de fórmula ( ce {C2H5} ), dando una fórmula molecular de ( ce {C4H10} ).
Debido a que los compuestos iónicos no contienen moléculas discretas, se usan fórmulas empíricas para indicar sus composiciones. Todos los compuestos, ya sean iónicos o covalentes, deben ser eléctricamente neutros. En consecuencia, las cargas positivas y negativas en una unidad de fórmula deben cancelarse exactamente entre sí. Si el catión y el anión tienen cargas de igual magnitud, como ( ce {Na ^ {+}} ) y ( ce {Cl ^ {-}} ), entonces el compuesto debe tener un 1: 1 proporción de cationes a aniones, y la fórmula empírica debe ser ( ce {NaCl} ). Si las cargas no son de la misma magnitud, entonces se necesita una relación catión: anión distinta de 1: 1 para producir un compuesto neutro. En el caso de ( ce {Mg ^ {2 +}} ) y ( ce {Cl ^ {-}} ), por ejemplo, se necesitan dos iones Cl – para equilibrar las dos cargas positivas en cada Mg 2 + ion, dando una fórmula empírica de ( ce {MgCl2} ). De manera similar, la fórmula para el compuesto iónico que contiene iones Na + y O 2− es Na 2 O.
Compuestos iónicos binarios
Un compuesto iónico que contiene solo dos elementos, uno presente como catión y otro como anión, se denomina compuesto iónico binario. Un ejemplo es ( ce {MgCl_2} ), un coagulante utilizado en la preparación de tofu a partir de soja. Para compuestos iónicos binarios, los subíndices en la fórmula empírica también se pueden obtener cruzando cargas: use el valor absoluto de la carga en un ion como subíndice para el otro ion. Este método se muestra esquemáticamente de la siguiente manera:
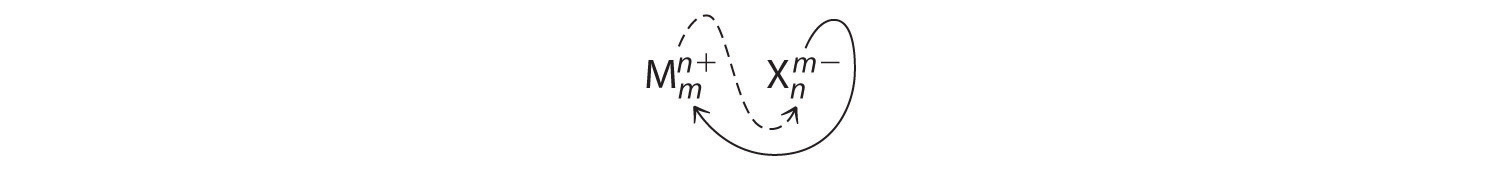
Al cruzar cargas, a veces es necesario reducir los subíndices a su relación más simple para escribir la fórmula empírica. Considere, por ejemplo, el compuesto formado por Mg 2 + y O 2− . El uso de los valores absolutos de las cargas en los iones como subíndices da la fórmula ( ce {Mg2O2} ):
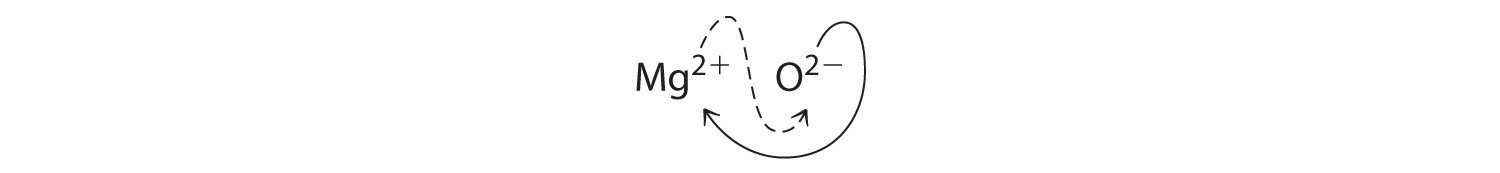
Esto simplifica a su correcta fórmula empírica MgO. La fórmula empírica tiene un Mg 2 + ion y un O 2− ion.
Iones poliatómicos
Los iones poliatómicos son grupos de átomos que llevan cargas eléctricas netas, aunque los átomos en un ion poliatómico se mantienen unidos por los mismos enlaces covalentes que mantienen unidos a los átomos en las moléculas. Así como hay muchos más tipos de moléculas que elementos simples, hay muchos más tipos de iones poliatómicos que iones monoatómicos. Dos ejemplos de cationes poliatómicos son el amonio (NH 4 + ) y el metilamonio (CH 3 NH 3 + [ 19459014]) iones. Los aniones poliatómicos son mucho más numerosos que los cationes poliatómicos; algunos ejemplos comunes están en Tabla ( PageIndex {1} ) .
| Fórmula | Nombre de Ion | Fórmula | Nombre de Ion |
|---|---|---|---|
| NH 4 + | amonio | HPO 4 2− | fosfato de hidrógeno |
| CH 3 NH 3 + | metilamonio | H 2 PO 4 – | fosfato de dihidrógeno |
| OH – | hidróxido | ClO – | hipoclorito |
| O 2 2− | peróxido | ClO 2 – | clorito |
| CN – | cianuro | ClO 3 – | clorato |
| SCN – | tiocianato | ClO 4 – | perclorato |
| NO 2 – | nitrito | MnO 4 – | permanganato |
| NO 3 – | nitrato | CrO4 2 – | cromato |
| CO 3 2− | carbonato | Cr 2 O 7 2− | dicromato |
| HCO 3 – | carbonato de hidrógeno o bicarbonato | C 2 O 4 2− | oxalato |
| SO 3 2− | sulfito | HCO 2 – | formiato |
| SO 4 2− | sulfato | CH 3 CO 2 – | acetato |
| HSO 4 – | sulfato de hidrógeno o bisulfato | C 6 H 5 CO 2 – | benzoato |
| PO 4 3− | fosfato |
El método utilizado para predecir las fórmulas empíricas para compuestos iónicos que contienen iones monoatómicos también se puede utilizar para compuestos que contienen iones poliatómicos. La carga general de los cationes debe equilibrar la carga general de los aniones en la unidad de fórmula. Por lo tanto, K + y NO 3 – los iones se combinan en una proporción 1: 1 para formar KNO 3 (nitrato de potasio o salitre) , un ingrediente importante en la pólvora negra. Del mismo modo, Ca 2 + y SO 4 2− forman CaSO 4 (sulfato de calcio), que combina con cantidades variables de agua para formar yeso y yeso de París. Los iones poliatómicos NH 4 + y NO 3 – forman NH 4 NO 3 [19459016 ] (nitrato de amonio), un fertilizante ampliamente utilizado y, en las manos equivocadas, un explosivo. Un ejemplo de un compuesto en el que los iones tienen cargas de diferentes magnitudes es el fosfato de calcio, que se compone de Ca 2 + y PO 4 3 – iones; Es un componente importante de los huesos. El compuesto es eléctricamente neutro porque los iones se combinan en una proporción de tres Ca 2 + iones [3 (+2) = +6] por cada dos iones [2 (−3) = −6], dando una fórmula empírica de Ca 3 (PO 4 ) 2 ; los paréntesis alrededor de PO 4 en la fórmula empírica indican que es un ion poliatómico. Escribir la fórmula para el fosfato de calcio como Ca 3 P 2 O 8 da el número correcto de cada átomo en la unidad de fórmula, pero oculta el hecho de que el el compuesto contiene iones PO 4 3− fácilmente identificables.
Hidratos
Muchos compuestos iónicos se presentan como hidratos, compuestos que contienen proporciones específicas de moléculas de agua unidas libremente, llamadas aguas de hidratación. Las aguas de hidratación a menudo se pueden eliminar simplemente calentando. Por ejemplo, el fosfato de dihidrógeno de calcio puede formar un sólido que contiene una molécula de agua por unidad ( ce {Ca (H2PO4) 2} ) y se utiliza como agente de fermentación en la industria alimentaria para provocar el aumento de los productos horneados. La fórmula empírica para el sólido es ( ce {Ca (H2PO4) 2 · H2O} ). En contraste, el sulfato de cobre generalmente forma un sólido azul que contiene cinco aguas de hidratación por unidad de fórmula, con la fórmula empírica ( ce {CuSO4 · 5H2O} ). Cuando se calienta, las cinco moléculas de agua se pierden, dando un sólido blanco con la fórmula empírica ( ce {CuSO4} ).


Los compuestos que difieren solo en el número de aguas de hidratación pueden tener propiedades muy diferentes. Por ejemplo, ( ce {CaSO4 · ½H2O} ) es yeso de París , que a menudo se usaba para hacer moldes resistentes para brazos o piernas rotas, mientras que ( ce {CaSO4 · 2H2O} ) es el yeso menos denso y escamoso, un mineral utilizado en paneles de paneles de yeso para la construcción de viviendas. Cuando se establece un yeso, una mezcla de yeso de París y agua cristaliza para dar un sólido ( ce {CaSO4 · 2H2O} ). Procesos similares se utilizan en el fraguado de cemento y hormigón.
Ácidos binarios
Algunos compuestos que contienen hidrógeno son miembros de una clase importante de sustancias conocidas como ácidos. La química de estos compuestos se explora con más detalle en capítulos posteriores de este texto, pero por ahora, será suficiente notar que muchos ácidos liberan iones de hidrógeno, H + , cuando se disuelven en agua. Para denotar esta propiedad química distintiva, una mezcla de agua con un ácido recibe un nombre derivado del nombre del compuesto. Si el compuesto es un ácido binario (compuesto de hidrógeno y otro elemento no metálico):
- La palabra “hidrógeno” se cambia al prefijo hidro-
- El otro nombre de elemento no metálico se modifica agregando el sufijo – ic
- La palabra “ácido” se agrega como segunda palabra
Por ejemplo, cuando el gas ( ce {HCl} ) (cloruro de hidrógeno) se disuelve en agua, la solución se llama ácido clorhídrico . Varios otros ejemplos de esta nomenclatura se muestran en la Tabla ( PageIndex {2} ).
| Nombre del gas | Nombre del ácido |
|---|---|
| HF ( g ), fluoruro de hidrógeno | HF ( aq ), ácido fluorhídrico |
| HCl ( g ), cloruro de hidrógeno | HCl ( aq ), ácido clorhídrico |
| HBr ( g ), bromuro de hidrógeno | HBr ( aq ), ácido bromhídrico |
| HI ( g ), yoduro de hidrógeno | HI ( aq ), ácido yodhídrico |
| H 2 S ( g ), sulfuro de hidrógeno | H 2 S ( aq ), ácido hidrosulfúrico |
Oxiácidos
Muchos compuestos que contienen tres o más elementos (como compuestos orgánicos o compuestos de coordinación) están sujetos a reglas de nomenclatura especializadas que aprenderá más adelante. Sin embargo, discutiremos brevemente los compuestos importantes conocidos como oxiácidos , compuestos que contienen hidrógeno, oxígeno y al menos otro elemento, y están unidos de tal manera que imparten propiedades ácidas al compuesto (usted aprenderá los detalles de esto en un capítulo posterior). Los oxiácidos típicos consisten en hidrógeno combinado con un ion poliatómico que contiene oxígeno. Para nombrar oxiácidos:
- Omitir “hidrógeno”
- Comienza con el nombre raíz del anión
- Reemplazar – comió con – ic , o – ite con – ous
- Agregar “ácido”
Por ejemplo, considere H 2 CO 3 (que podría tener la tentación de llamar “carbonato de hidrógeno”). Para nombrar esto correctamente, se omite “hidrógeno”; el – comió de carbonato se reemplaza con – ic ; y se agrega ácido, entonces su nombre es ácido carbónico. Otros ejemplos se dan en la Tabla ( PageIndex {3} ). Hay algunas excepciones al método de denominación general (p. Ej., H 2 SO 4 se llama ácido sulfúrico, no ácido sulfúrico, y H 2 SO 3 es sulfuroso, no sulfoso, ácido).
| Fórmula | Nombre del anión | Nombre ácido |
|---|---|---|
| HC 2 H 3 O 2 | acetato | ácido acético |
| HNO 3 | nitrato | ácido nítrico |
| HNO 2 | nitrito | ácido nitroso |
| HClO 4 | perclorato | ácido perclórico |
| H 2 CO 3 | carbonato | ácido carbónico |
| H 2 SO 4 | sulfato | ácido sulfúrico |
| H 2 SO 3 | sulfito | ácido sulfuroso |
| H 3 PO 4 | fosfato | ácido fosfórico |
Bases
Presentaremos definiciones más completas de bases en capítulos posteriores, pero prácticamente cada base que encuentre mientras tanto será un compuesto iónico, como el hidróxido de sodio (NaOH) y el hidróxido de bario [Ba (OH) 2 [ 19459016]], que contiene el ion hidróxido y un catión metálico. Estos tienen la fórmula general M (OH) n . Es importante reconocer que los alcoholes, con la fórmula general ROH, son compuestos covalentes, no compuestos iónicos; en consecuencia, no se disocian en agua para formar una solución básica (que contiene iones OH – ). Cuando una base reacciona con cualquiera de los ácidos que hemos discutido, acepta un protón (H + ). Por ejemplo, el ion hidróxido (OH – ) acepta un protón para formar H 2 O. Por lo tanto, las bases también se denominan aceptores de protones [ 19459071].
Las soluciones acuosas concentradas de amoníaco (NH 3 ) contienen cantidades significativas del ion hidróxido, aunque la sustancia disuelta es no principalmente hidróxido de amonio (NH 4 OH) como se indica a menudo en la etiqueta. Por lo tanto, la solución acuosa de amoniaco también es una base común. Reemplazar un átomo de hidrógeno de NH 3 con un grupo alquilo da como resultado una amina (RNH 2 ), que también es una base. Las aminas tienen olores fuertes, por ejemplo, la metilamina (CH 3 NH 2 ) es uno de los compuestos responsables del mal olor asociado con el pescado en mal estado. La importancia fisiológica de las aminas se sugiere en la palabra vitamina , que se deriva de la frase aminas vitales . La palabra fue acuñada para describir sustancias dietéticas que fueron efectivas para prevenir el escorbuto, el raquitismo y otras enfermedades porque se suponía que estas sustancias eran aminas. Posteriormente, se ha confirmado que algunas vitaminas son aminas.
Compuestos inorgánicos binarios
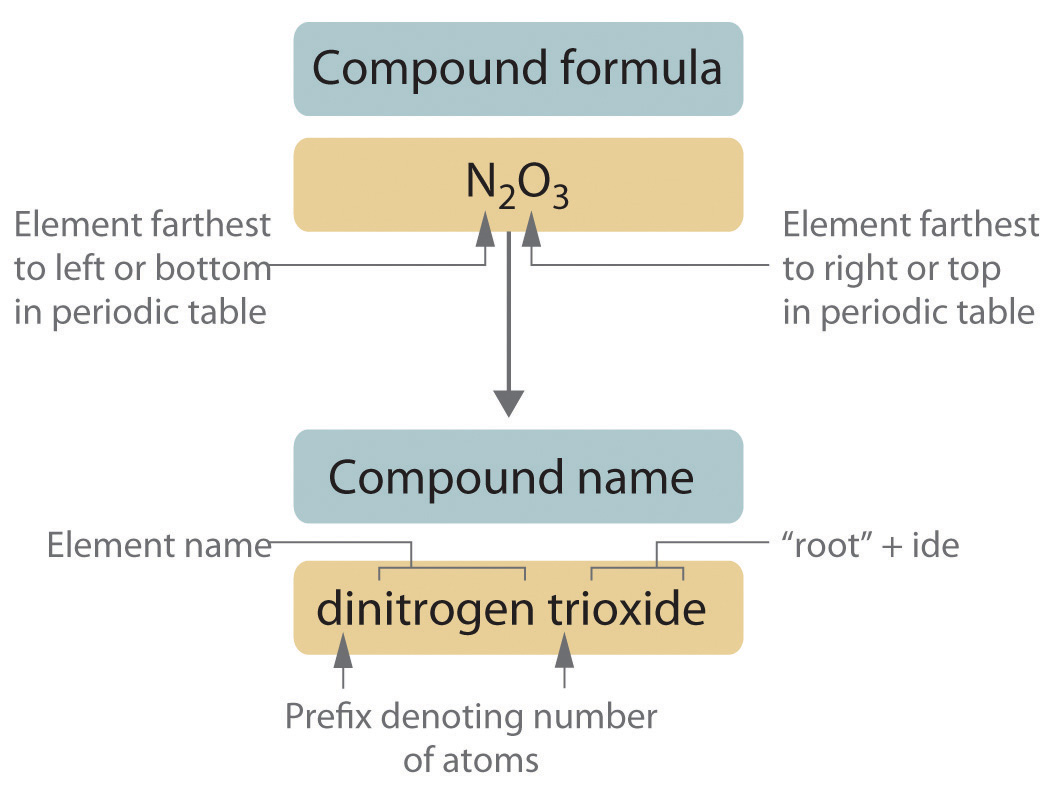
Los compuestos covalentes binarios —compuestos covalentes que contienen solo dos elementos— se nombran utilizando un procedimiento similar al utilizado para los compuestos iónicos simples, pero se agregan prefijos según sea necesario para indicar el número de átomos de cada tipo . El procedimiento, diagramado en Figura ( PageIndex {2} ) consta de los siguientes pasos:
-
Coloque los elementos en su orden correcto.
- El elemento más alejado a la izquierda en la tabla periódica generalmente se nombra primero. Si ambos elementos están en el mismo grupo, el elemento más cercano a la parte inferior de la columna se nombra primero.
- El segundo elemento se nombra como si fuera un anión monoatómico en un compuesto iónico (aunque no lo sea), con el sufijo -ide adjunto a la raíz del nombre del elemento.
-
Identifica el número de cada tipo de átomo presente.
-
Los prefijos derivados de tallos griegos se usan para indicar el número de cada tipo de átomo en la unidad de fórmula ( Tabla ( PageIndex {3} )) . El prefijo mono – (“uno”) se usa solo cuando es absolutamente necesario para evitar confusiones, así como el subíndice 1 se omite al escribir fórmulas moleculares.
Para demostrar los pasos 1 y 2a, el HCl se denomina cloruro de hidrógeno (porque el hidrógeno está a la izquierda del cloro en la tabla periódica), y PCl 5 es el pentacloruro de fósforo. El orden de los elementos a nombre de BrF 3 , trifluoruro de bromo, está determinado por el hecho de que el bromo se encuentra por debajo del flúor en el Grupo 17.
Tabla ( PageIndex {3} ): Prefijos para indicar el número de átomos en nombres químicos Prefijo Número mono- 1 di- 2 tri- 3 tetra- 4 penta- 5 hexa- 6 hepta- 7 octa- 8 nona- 9 deca- 10 undeca- 11 dodeca- 12 - If a molecule contains more than one atom of both elements, then prefixes are used for both. Thus N 2 O 3 is di nitrogen tri oxide, as shown in Figure 2.13 .
- In some names, the final a or o of the prefix is dropped to avoid awkward pronunciation. Thus OsO 4 is osmium tetroxide rather than osmium tetraoxide.
-
-
Write the name of the compound.
- Binary compounds of the elements with oxygen are generally named as “element oxide,” with prefixes that indicate the number of atoms of each element per formula unit. For example, CO is carbon monoxide. The only exception is binary compounds of oxygen with fluorine, which are named as oxygen fluorides.
- Certain compounds are always called by the common names that were assigned before formulas were used. For example, H 2 O is water (not dihydrogen oxide); NH 3 is ammonia; PH 3 is phosphine; SiH 4 is silane; and B 2 H 6 , a dimer of BH 3 , is diborane. For many compounds, the systematic name and the common name are both used frequently, requiring familiarity with both. For example, the systematic name for NO is nitrogen monoxide, but it is much more commonly called nitric oxide. Similarly, N 2 O is usually called nitrous oxide rather than dinitrogen monoxide. Notice that the suffixes – ic and – ous are the same ones used for ionic compounds.
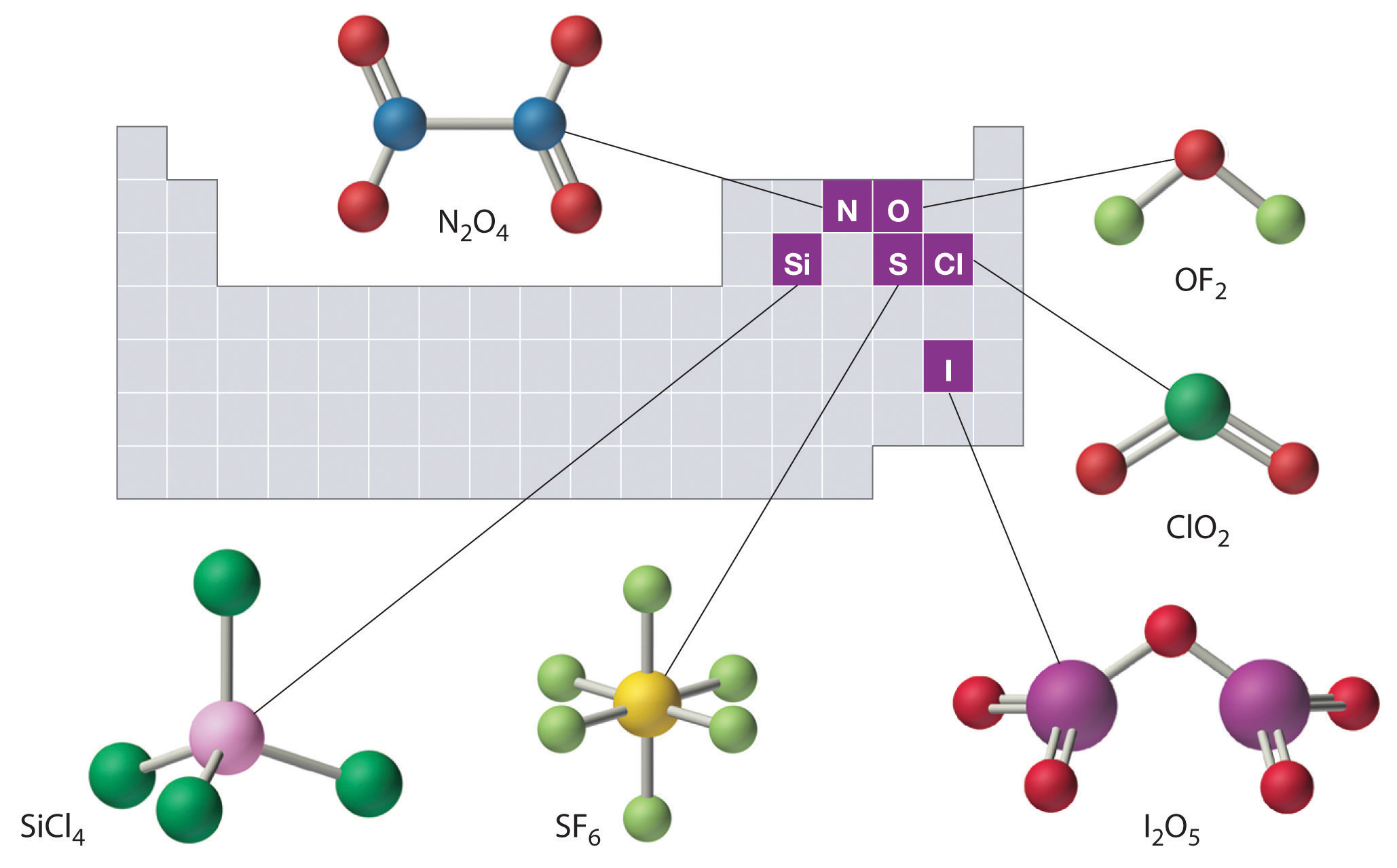
The structures of some of the compounds in Examples (PageIndex{3}) and (PageIndex{4}) are shown in Figure (PageIndex{2}) along with the location of the “central atom” of each compound in the periodic table. It may seem that the compositions and structures of such compounds are entirely random, but this is not true. After mastering the material discussed later on this course, one is able to predict the compositions and structures of compounds of this type with a high degree of accuracy.
Summary
The composition of a compound is represented by an empirical or molecular formula, each consisting of at least one formula unit. Covalent inorganic compounds are named using a procedure similar to that used for ionic compounds, whereas hydrocarbons use a system based on the number of bonds between carbon atoms. Covalent inorganic compounds are named by a procedure similar to that used for ionic compounds, using prefixes to indicate the numbers of atoms in the molecular formula. An empirical formula gives the relative numbers of atoms of the elements in a compound, reduced to the lowest whole numbers. The formula unit is the absolute grouping represented by the empirical formula of a compound, either ionic or covalent. Empirical formulas are particularly useful for describing the composition of ionic compounds, which do not contain readily identifiable molecules. Some ionic compounds occur as hydrates, which contain specific ratios of loosely bound water molecules called waters of hydration.