Las tres fases (o estados) comunes de la materia son gases, líquidos y sólidos. Los gases tienen la menor densidad de los tres, son altamente compresibles y llenan completamente cualquier contenedor en el que se colocan. Los gases se comportan de esta manera porque sus fuerzas intermoleculares son relativamente débiles, por lo que sus moléculas se mueven constantemente independientemente de las otras moléculas presentes. Los sólidos, en contraste, son relativamente densos, rígidos e incompresibles porque sus fuerzas intermoleculares son tan fuertes que las moléculas están esencialmente bloqueadas en su lugar. Los líquidos son relativamente densos e incompresibles, como los sólidos, pero fluyen fácilmente para adaptarse a la forma de sus recipientes, como los gases. Por lo tanto, podemos concluir que la suma de las fuerzas intermoleculares en los líquidos se encuentra entre las de los gases y los sólidos. La figura ( PageIndex {1} ) compara los tres estados de la materia e ilustra las diferencias a nivel molecular.
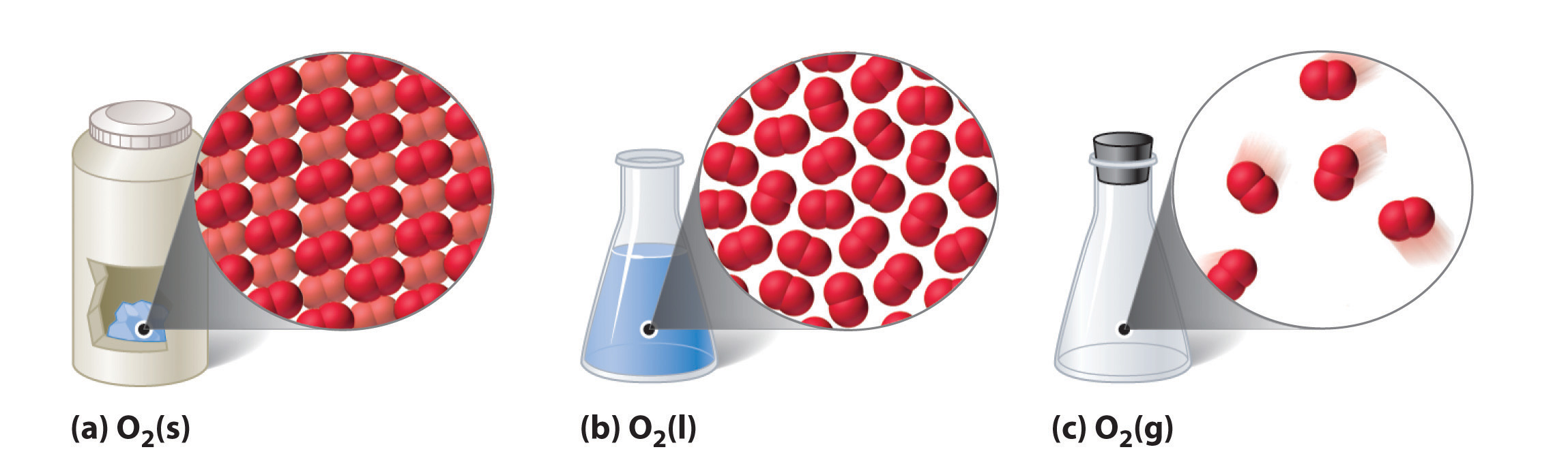
El estado de una sustancia dada depende en gran medida de las condiciones. Por ejemplo, H 2 O se encuentra comúnmente en los tres estados: hielo sólido, agua líquida y vapor de agua (su forma gaseosa). En la mayoría de las condiciones, encontramos el agua como el líquido que es esencial para la vida; lo bebemos, cocinamos con él y nos bañamos en él. Cuando la temperatura es lo suficientemente fría como para transformar el líquido en hielo, podemos esquiar o patinar sobre él, empacarlo en una bola de nieve o cono de nieve e incluso construir viviendas con él. Vapor de agua ( el término vapor se refiere a la forma gaseosa de una sustancia que es un líquido o un sólido en condiciones normales, entonces nitrógeno (N 2 ) y el oxígeno (O 2 ) se denominan gases, pero el agua gaseosa en la atmósfera se llama vapor de agua) es un componente del aire que respiramos y se produce cada vez que calentamos agua para cocinar o preparar café o té. El vapor de agua a temperaturas superiores a 100 ° C se denomina vapor. El vapor se utiliza para conducir maquinaria grande, incluidas turbinas que generan electricidad. Las propiedades de los tres estados del agua se resumen en la Tabla 10.1.
| Temperatura | Estado | Densidad (g / cm3) |
|---|---|---|
| ≤0 ° C | sólido (hielo) | 0.9167 (a 0.0 ° C) |
| 0 ° C – 100 ° C | líquido (agua) | 0.9997 (a 4.0 ° C) |
| ≥100 ° C | vapor (vapor) | 0,005476 (a 127 ° C) |
La estructura geométrica y las propiedades físicas y químicas de los átomos, iones y moléculas generalmente no dependen de su estado físico; Las moléculas de agua individuales en hielo, agua líquida y vapor, por ejemplo, son todas idénticas. Por el contrario, las propiedades macroscópicas de una sustancia dependen en gran medida de su estado físico, que está determinado por las fuerzas y condiciones intermoleculares, como la temperatura y la presión.
La Figura ( PageIndex {2} ) muestra las ubicaciones en la tabla periódica de los elementos que se encuentran comúnmente en los estados gaseoso, líquido y sólido. A excepción del hidrógeno, los elementos que ocurren naturalmente como gases están en el lado derecho de la tabla periódica. De estos, todos los gases nobles (grupo 18) son gases monoatómicos, mientras que los otros elementos gaseosos son moléculas diatómicas ( H 2 , N 2 , O 2 , F 2 y Cl 2 ). El oxígeno también puede formar un segundo alótropo, la molécula triatómica altamente reactiva del ozono ( O 3 ), que también es un gas. En contraste, el bromo (como Br 2 ) y el mercurio (Hg) son líquidos en condiciones normales (25 ° C y 1.0 atm, comúnmente conocidos como “temperatura y presión ambiente”). El galio (Ga), que se derrite a solo 29.76 ° C, puede convertirse en un líquido simplemente sosteniendo un recipiente en la mano o manteniéndolo en una habitación sin aire acondicionado en un caluroso día de verano. El resto de los elementos son todos sólidos en condiciones normales.
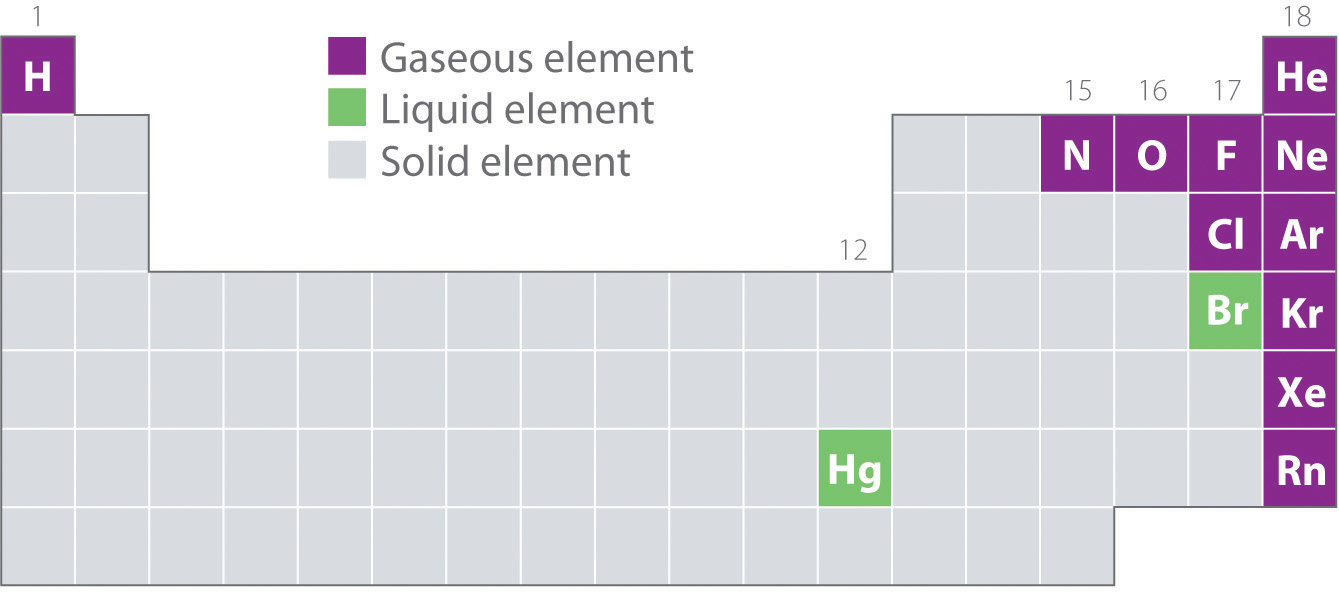
Todos los elementos gaseosos (excepto los gases nobles monoatómicos) son moléculas. W dentro del mismo grupo (1, 15, 16 y 17), los elementos más ligeros son gases. Todas las sustancias gaseosas se caracterizan por interacciones débiles entre las moléculas o átomos constituyentes.
Resumen
La materia a granel puede existir en tres estados: gas, líquido y sólido. Los gases tienen la menor densidad de los tres, son altamente compresibles y llenan sus contenedores por completo. Los elementos que existen como gases a temperatura y presión ambiente se agrupan en el lado derecho de la tabla periódica; se presentan como gases monoatómicos (gases nobles) o moléculas diatómicas (algunos halógenos, N 2 , O 2 ).