Las propiedades de los líquidos son intermedias entre las de los gases y los sólidos, pero son más similares a los sólidos. A diferencia de las fuerzas moleculares intra , como los enlaces covalentes que mantienen los átomos juntos en las moléculas y los iones poliatómicos, inter las fuerzas moleculares mantienen las moléculas juntas en un líquido o sólido. Las fuerzas intermoleculares son generalmente mucho más débiles que los enlaces covalentes. Por ejemplo, se requieren 927 kJ para superar las fuerzas intramoleculares y romper ambos enlaces O-H en 1 mol de agua, pero solo se necesitan unos 41 kJ para superar las atracciones intermoleculares y convertir 1 mol de agua líquida en vapor de agua a 100 ° C. (¡A pesar de este valor aparentemente bajo, las fuerzas intermoleculares en el agua líquida se encuentran entre las fuerzas más fuertes conocidas!) Dada la gran diferencia en las fuerzas de las fuerzas intra e intermoleculares, los cambios entre los estados sólido, líquido y gaseoso ocurren casi invariablemente para sustancias moleculares sin romper enlaces covalentes .
Las propiedades de los líquidos son intermedias entre las de los gases y los sólidos, pero son más similares a los sólidos.
Las fuerzas intermoleculares determinan las propiedades de volumen como los puntos de fusión de los sólidos y los puntos de ebullición de los líquidos. Los líquidos hierven cuando las moléculas tienen suficiente energía térmica para superar las fuerzas de atracción intermoleculares que las mantienen juntas, formando así burbujas de vapor dentro del líquido. Del mismo modo, los sólidos se derriten cuando las moléculas adquieren suficiente energía térmica para vencer las fuerzas intermoleculares que las fijan en el sólido.
Las fuerzas intermoleculares son de naturaleza electrostática; es decir, surgen de la interacción entre especies cargadas positiva y negativamente. Al igual que los enlaces iónicos y covalentes, las interacciones intermoleculares son la suma de componentes atractivos y repulsivos. Debido a que las interacciones electrostáticas disminuyen rápidamente al aumentar la distancia entre las moléculas, las interacciones intermoleculares son más importantes para los sólidos y líquidos, donde las moléculas están muy juntas. Estas interacciones se vuelven importantes para los gases solo a presiones muy altas, donde son responsables de las desviaciones observadas de la ley de gases ideal a altas presiones. (Para obtener más información sobre el comportamiento de los gases reales y las desviaciones de la ley del gas ideal).
En esta sección, consideramos explícitamente tres tipos de interacciones intermoleculares: Hay dos tipos adicionales de interacción electrostática con los que ya está familiarizado: las interacciones ión-ión responsables del enlace iónico y el dipolo iónico interacciones que ocurren cuando las sustancias iónicas se disuelven en una sustancia polar como el agua. Los dos primeros a menudo se describen colectivamente como fuerzas de van der Waals .
Interacciones dipolo-dipolo
Los enlaces covalentes polares se comportan como si los átomos unidos tienen cargas fraccionadas localizadas que son iguales pero opuestas (es decir, los dos átomos unidos generan un dipolo ). Si la estructura de una molécula es tal que los dipolos de enlace individuales no se cancelan entre sí, entonces la molécula tiene un momento dipolar neto. Las moléculas con momentos dipolares netos tienden a alinearse de manera que el extremo positivo de un dipolo está cerca del extremo negativo de otro y viceversa, como se muestra en la Figura ( PageIndex {1a} ).
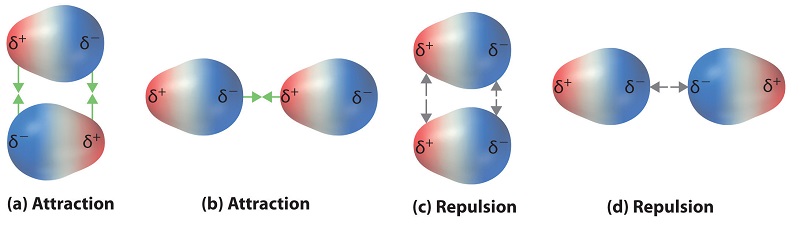
Estas disposiciones son más estables que las disposiciones en las que dos extremos positivos o dos negativos son adyacentes (Figura ( PageIndex {1c} )). Por lo tanto, interacciones dipolo-dipolo , como las de la Figura ( PageIndex {1b} ), son interacciones intermoleculares atractivas , mientras que las de la Figura ( PageIndex {1d} ) son interacciones intermoleculares repulsivas . Debido a que las moléculas en un líquido se mueven libremente y continuamente, las moléculas siempre experimentan interacciones dipolo-dipolo atractivas y repulsivas simultáneamente, como se muestra en la Figura ( PageIndex {2} ). En promedio, sin embargo, las interacciones atractivas dominan.
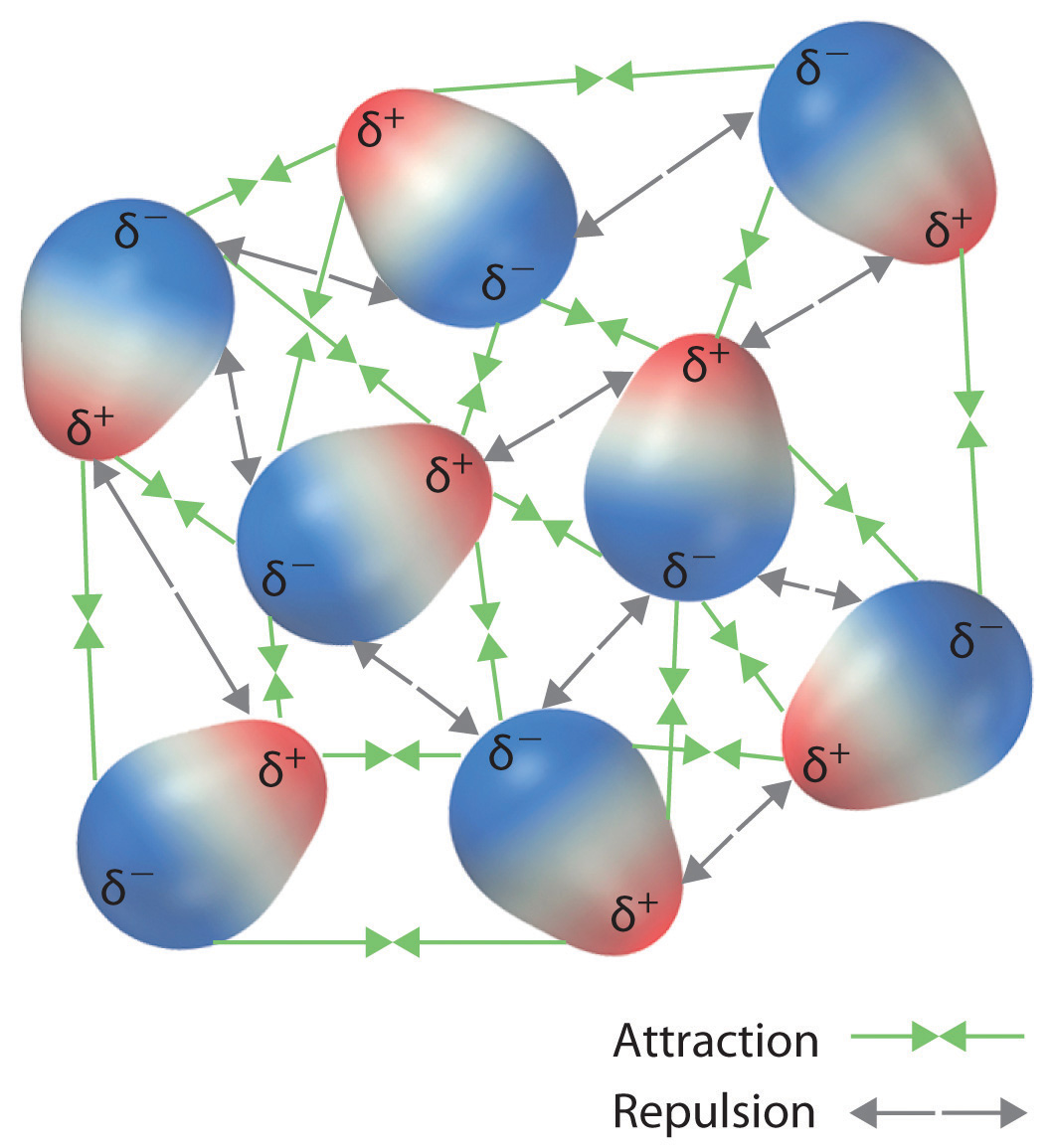
Debido a que cada extremo de un dipolo posee solo una fracción de la carga de un electrón, las interacciones dipolo-dipolo son sustancialmente más débiles que las interacciones entre dos iones, cada uno de los cuales tiene una carga de al menos ± 1, o entre un dipolo y un ion, en el que una de las especies tiene al menos una carga positiva o negativa completa. Además, la interacción atractiva entre los dipolos disminuye mucho más rápidamente al aumentar la distancia que las interacciones ión-ión. Recuerde que la energía atractiva entre dos iones es proporcional a 1 / r , donde r es la distancia entre los iones. Duplicar la distancia ( r → 2 r ) disminuye la energía atractiva a la mitad. En contraste, la energía de la interacción de dos dipolos es proporcional a 1 / r 3 , por lo que duplicar la distancia entre los dipolos disminuye la fuerza de la interacción en 2 3 , o 8 veces. Por lo tanto, una sustancia como ( ce {HCl} ), que se mantiene parcialmente unida por interacciones dipolo-dipolo, es un gas a temperatura ambiente y 1 atm de presión, mientras que ( ce {NaCl} ), que es unido por interacciones interiónicas, es un sólido de alto punto de fusión. Dentro de una serie de compuestos de masa molar similar, la fuerza de las interacciones intermoleculares aumenta a medida que aumenta el momento dipolar de las moléculas, como se muestra en la Tabla ( PageIndex {1} ).
| Compuesto | Masa molar (g / mol) | Momento dipolar (D) | Punto de ebullición (K) |
|---|---|---|---|
| C 3 H 6 (ciclopropano) | 42 | 0 | 240 |
| CH 3 OCH 3 (éter dimetílico) | 46 | 1,30 | 248 |
| CH 3 CN (acetonitrilo) | 41 | 3,9 | 355 |
La energía atractiva entre dos iones es proporcional a 1 / r, mientras que la energía atractiva entre dos dipolos es proporcional a 1 / r6.
Fuerzas de dispersión de Londres
Hasta ahora solo hemos considerado las interacciones entre las moléculas polares, pero se deben considerar otros factores para explicar por qué muchas moléculas no polares, como el bromo, el benceno y el hexano, son líquidos a temperatura ambiente y otros, como el yodo y el naftaleno , son sólidos. Incluso los gases nobles se pueden licuar o solidificar a bajas temperaturas, altas presiones o ambas (Tabla ( PageIndex {2} )).
¿Qué tipo de fuerzas atractivas pueden existir entre moléculas o átomos no polares? Fritz London (1900–1954), un físico alemán que más tarde trabajó en los Estados Unidos, respondió a esta pregunta. En 1930, Londres propuso que las fluctuaciones temporales en las distribuciones de electrones dentro de los átomos y las moléculas no polares podrían dar lugar a la formación de momentos dipolares instantáneos de corta duración , que producen fuerzas atractivas llamadas fuerzas de dispersión de Londres entre sustancias no polares.
| Sustancia | Masa molar (g / mol) | Punto de fusión (° C) | Punto de ebullición (° C) |
|---|---|---|---|
| Ar | 40 | −189,4 | −185,9 |
| Xe | 131 | −111,8 | −108,1 |
| N 2 | 28 | −210 | −195,8 |
| O 2 | 32 | −218,8 | −183,0 |
| F 2 | 38 | −219,7 | −188,1 |
| I 2 | 254 | 113,7 | 184,4 |
| CH 4 | 16 | −182,5 | −161,5 |
Considere un par de átomos de He adyacentes, por ejemplo. En promedio, los dos electrones en cada átomo de He están distribuidos uniformemente alrededor del núcleo. Sin embargo, debido a que los electrones están en movimiento constante, es probable que su distribución en un átomo sea asimétrica en cualquier instante dado, lo que resulta en un momento dipolar instantáneo. Como se muestra en la parte (a) en la Figura ( PageIndex {3} ), el momento dipolar instantáneo en un átomo puede interactuar con los electrones en un átomo adyacente, empujándolos hacia el extremo positivo del dipolo instantáneo o repeliéndolos El final negativo. El efecto neto es que el primer átomo causa la formación temporal de un dipolo, llamado dipolo inducido , en el segundo. Las interacciones entre estos dipolos temporales hacen que los átomos se atraigan entre sí. Estas interacciones atractivas son débiles y se caen rápidamente al aumentar la distancia. London pudo demostrar con la mecánica cuántica que la energía atractiva entre las moléculas debido a interacciones dipolo inducidas por dipolos temporales cae como 1 / r 6 . Duplicar la distancia, por lo tanto, disminuye la energía atractiva en 2 6 , o 64 veces.
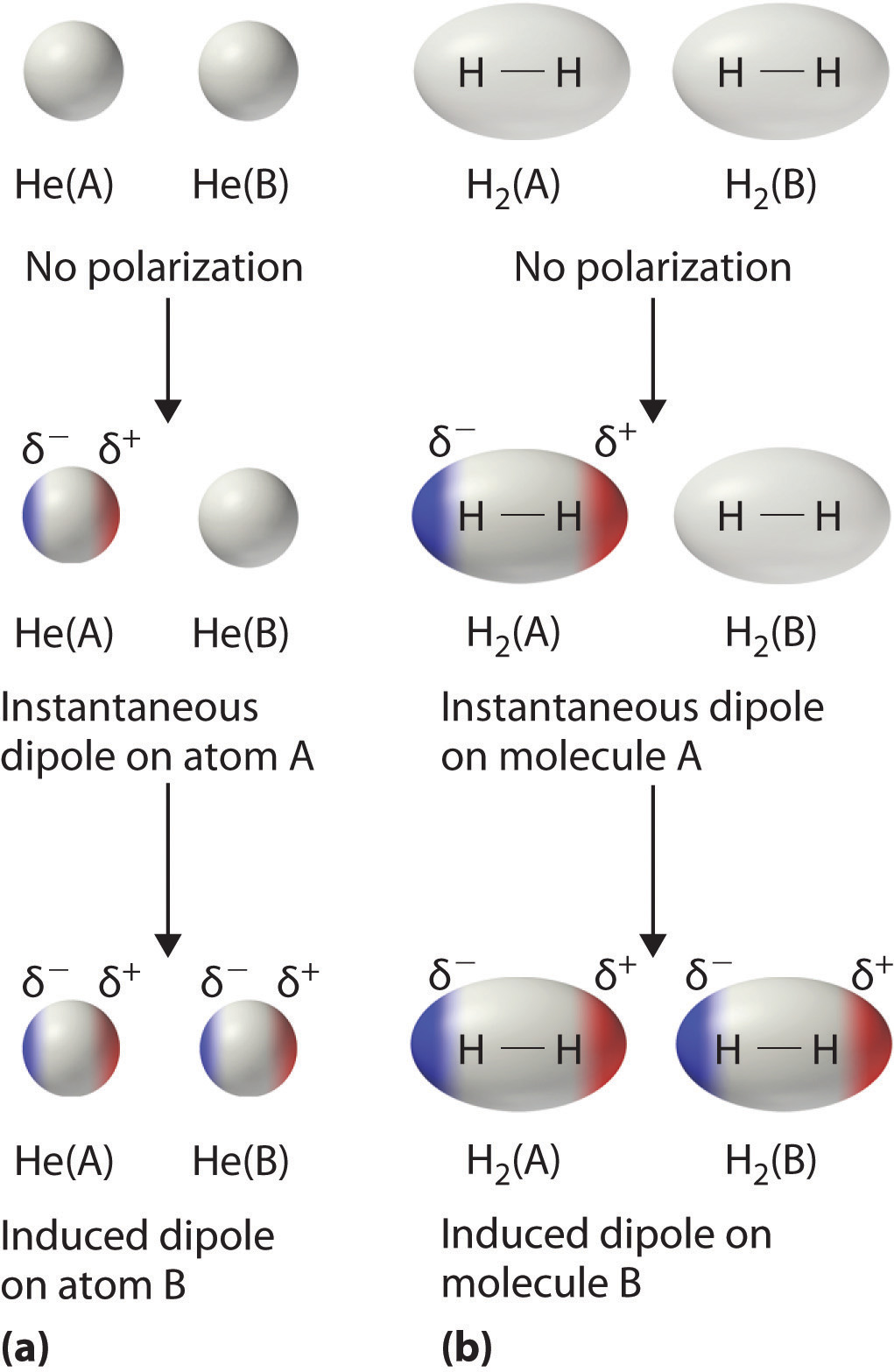
Las interacciones dipolo inducidas por dipolos instantáneos entre moléculas no polares pueden producir atracciones intermoleculares al igual que producen atracciones interatómicas en sustancias monoatómicas como Xe. Este efecto, ilustrado para dos moléculas H 2 en la parte (b) en la Figura ( PageIndex {3} ), tiende a ser más pronunciado a medida que aumentan las masas atómicas y moleculares (Tabla ( PageIndex { 2} )). Por ejemplo, Xe hierve a −108.1 ° C, mientras que hierve a −269 ° C. La razón de esta tendencia es que la fuerza de las fuerzas de dispersión de Londres está relacionada con la facilidad con la que puede perturbarse la distribución de electrones en un átomo dado. En átomos pequeños como He, los dos electrones 1 se mantienen cerca del núcleo en un volumen muy pequeño, y las repulsiones electrón-electrón son lo suficientemente fuertes como para evitar una asimetría significativa en su distribución. Sin embargo, en átomos más grandes como Xe, los electrones externos son mucho menos atraídos por el núcleo debido a las capas intermedias llenas. Como resultado, es relativamente fácil deformar temporalmente la distribución de electrones para generar un dipolo instantáneo o inducido. La facilidad de deformación de la distribución de electrones en un átomo o molécula se llama polarización . Debido a que la distribución de electrones se perturba más fácilmente en especies grandes y pesadas que en especies pequeñas y ligeras, decimos que las sustancias más pesadas tienden a ser mucho más polarizables que las más ligeras.
Para sustancias similares, las fuerzas de dispersión de Londres se hacen más fuertes al aumentar el tamaño molecular.
La polarización de una sustancia también determina cómo interactúa con iones y especies que poseen dipolos permanentes. Así, las fuerzas de dispersión de Londres son responsables de la tendencia general hacia puntos de ebullición más altos con mayor masa molecular y mayor área superficial en una serie homóloga de compuestos, como los alcanos (parte (a) en la Figura ( PageIndex {4} )) . Las fuerzas de las fuerzas de dispersión de Londres también dependen significativamente de la forma molecular porque la forma determina qué cantidad de una molécula puede interactuar con sus moléculas vecinas en un momento dado. Por ejemplo, la parte (b) en la Figura ( PageIndex {4} ) muestra 2,2-dimetilpropano (neopentano) y n -pentano, los cuales tienen la fórmula empírica C 5 H 12 . El neopentano es casi esférico, con un área de superficie pequeña para las interacciones intermoleculares, mientras que n -pentano tiene una conformación extendida que le permite entrar en contacto cercano con otras moléculas de n -pentano. Como resultado, el punto de ebullición del neopentano (9.5 ° C) es más de 25 ° C más bajo que el punto de ebullición del n -pentano (36.1 ° C).
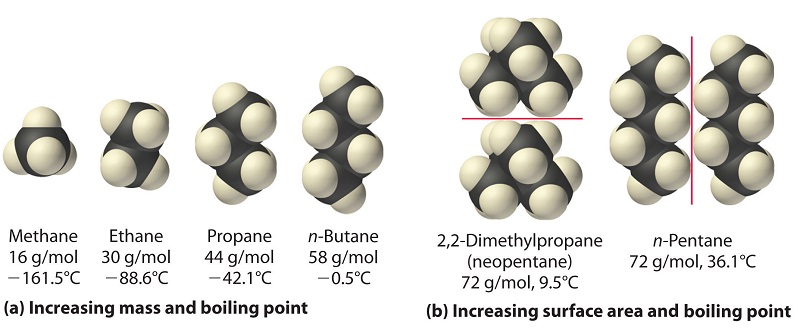
Todas las moléculas, ya sean polares o no polares, son atraídas entre sí por las fuerzas de dispersión de Londres, además de cualquier otra fuerza atractiva que pueda estar presente. En general, sin embargo, las interacciones dipolo-dipolo en moléculas polares pequeñas son significativamente más fuertes que las fuerzas de dispersión de Londres, por lo que predominan las primeras.
Enlaces de hidrógeno
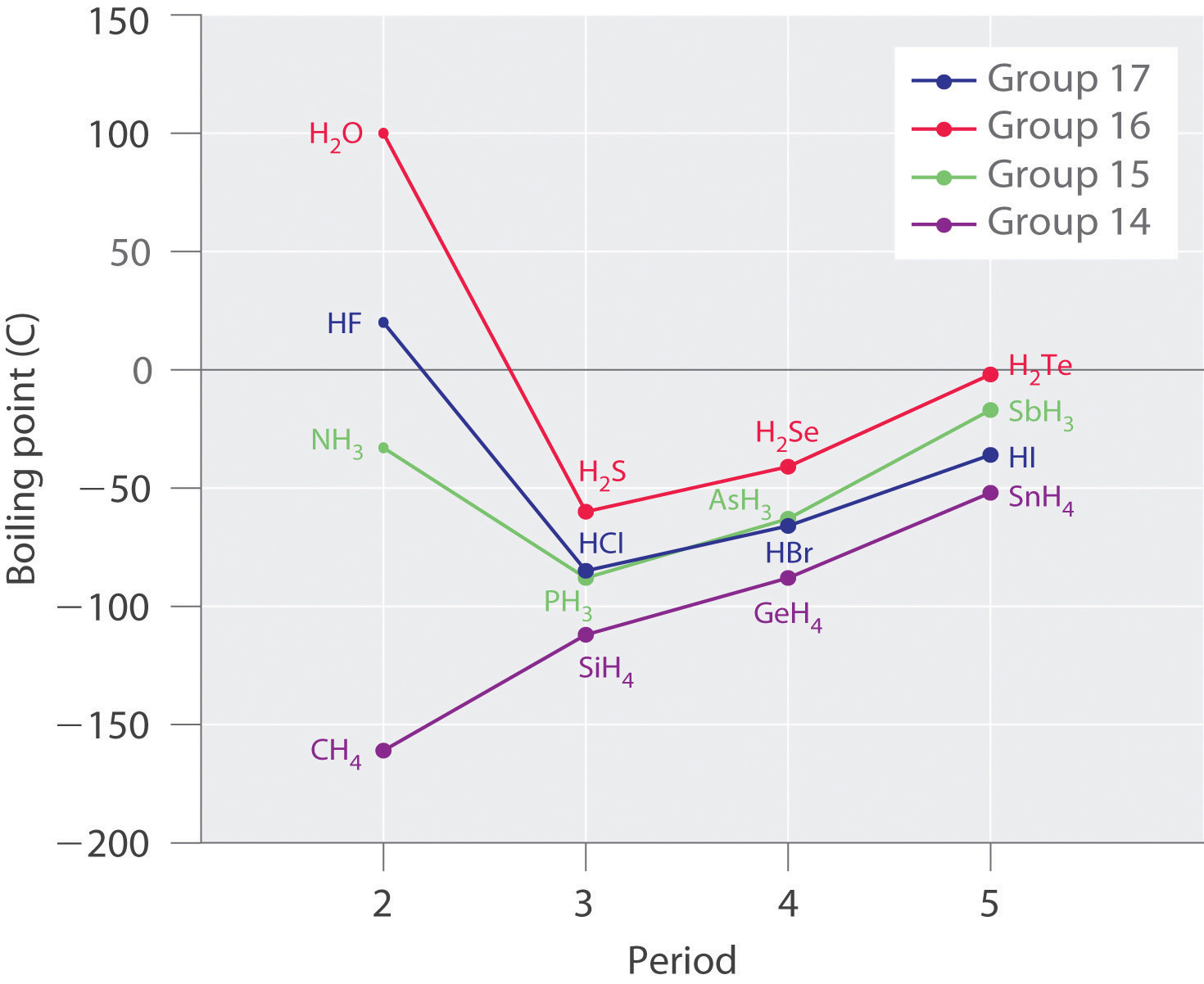
Las moléculas con átomos de hidrógeno unidos a átomos electronegativos como O, N y F (y en mucho menor medida Cl y S) tienden a exhibir interacciones intermoleculares inusualmente fuertes. Esto da como resultado puntos de ebullición mucho más altos que los observados para sustancias en las que dominan las fuerzas de dispersión de Londres, como se ilustra para los hidruros covalentes de elementos de los grupos 14-17 en la Figura ( PageIndex {5} ). El metano y sus congéneres más pesados en el grupo 14 forman una serie cuyos puntos de ebullición aumentan suavemente con el aumento de la masa molar. Esta es la tendencia esperada en las moléculas no polares, para las cuales las fuerzas de dispersión de Londres son las fuerzas intermoleculares exclusivas. Por el contrario, los hidruros de los miembros más ligeros de los grupos 15-17 tienen puntos de ebullición que son más de 100 ° C mayores de lo previsto en función de sus masas molares. El efecto es más dramático para el agua: si extendemos la línea recta que conecta los puntos para H 2 Te y H 2 Se a la línea para el período 2, obtenemos un punto de ebullición estimado de −130 ° C para agua! Imagine las implicaciones para la vida en la Tierra si el agua hierve a -130 ° C en lugar de 100 ° C.
¿Por qué las fuerzas intermoleculares fuertes producen puntos de ebullición tan anómalamente altos y otras propiedades inusuales, tales como altas entalpías de vaporización y altos puntos de fusión? La respuesta radica en la naturaleza altamente polar de los enlaces entre el hidrógeno y elementos muy electronegativos como O, N y F. La gran diferencia en la electronegatividad resulta en una gran carga positiva parcial en el hidrógeno y una carga negativa parcial correspondiente en el O , N o F átomo. En consecuencia, los enlaces H – O, H – N y H – F tienen dipolos de enlace muy grandes que pueden interactuar fuertemente entre sí. Debido a que un átomo de hidrógeno es tan pequeño, estos dipolos también pueden acercarse entre sí más de cerca que la mayoría de los otros dipolos. La combinación de dipolos de enlaces grandes y distancias cortas dipolo-dipolo da como resultado interacciones muy fuertes dipolo-dipolo llamadas enlaces de hidrógeno , como se muestra para el hielo en la Figura ( PageIndex {6} ). Un enlace de hidrógeno generalmente se indica mediante una línea de puntos entre el átomo de hidrógeno unido a O, N o F (el donante de enlace de hidrógeno ) y el átomo que tiene el único par de electrones (el hidrógeno aceptador de bonos ). Debido a que cada molécula de agua contiene dos átomos de hidrógeno y dos pares solitarios, una disposición tetraédrica maximiza el número de enlaces de hidrógeno que se pueden formar. En la estructura del hielo, cada átomo de oxígeno está rodeado por un tetraedro distorsionado de átomos de hidrógeno que forman puentes hacia los átomos de oxígeno de las moléculas de agua adyacentes. Sin embargo, los átomos de hidrógeno puente no son equidistantes de los dos átomos de oxígeno que conectan. En cambio, cada átomo de hidrógeno es 101 pm de un oxígeno y 174 pm del otro. En contraste, cada átomo de oxígeno está unido a dos átomos de H a la distancia más corta y dos a la distancia más larga, lo que corresponde a dos enlaces covalentes O-H y dos enlaces de hidrógeno O⋅⋅⋅H de moléculas de agua adyacentes, respectivamente. La estructura de hielo abierta y cagelica resultante significa que el sólido es en realidad un poco menos denso que el líquido, lo que explica por qué el hielo flota en el agua en lugar de hundirse.
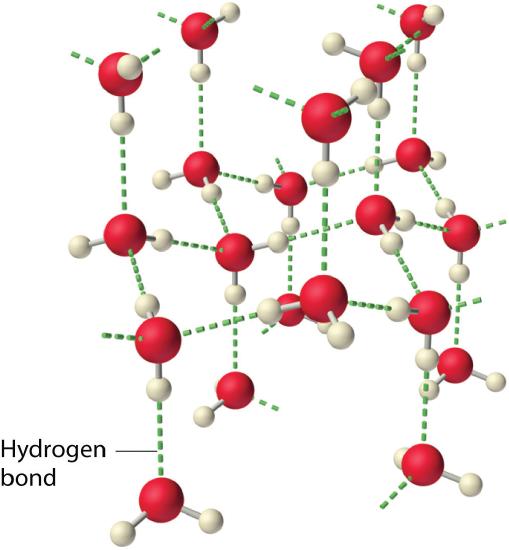
Cada molécula de agua acepta dos enlaces de hidrógeno de otras dos moléculas de agua y dona dos átomos de hidrógeno para formar enlaces de hidrógeno con dos moléculas de agua más, produciendo una estructura abierta similar a un cagel. La estructura del agua líquida es muy similar, pero en el líquido, los enlaces de hidrógeno se rompen y forman continuamente debido al rápido movimiento molecular.
La formación de enlaces de hidrógeno requiere un donante de enlaces de hidrógeno y un aceptor de enlaces de hidrógeno.
Debido a que el hielo es menos denso que el agua líquida, los ríos, lagos y océanos se congelan de arriba hacia abajo. De hecho, el hielo forma una capa superficial protectora que aísla el resto del agua, permitiendo que los peces y otros organismos sobrevivan en los niveles inferiores de un lago o mar congelado. Si el hielo fuera más denso que el líquido, el hielo formado en la superficie en clima frío se hundiría tan rápido como se formó. Las masas de agua se congelarían de abajo hacia arriba, lo que sería letal para la mayoría de las criaturas acuáticas. La expansión del agua cuando se congela también explica por qué los motores de automóviles o botes deben protegerse con “anticongelante” y por qué las tuberías sin protección en las casas se rompen si se les permite congelar.
Aunque los enlaces de hidrógeno son significativamente más débiles que los enlaces covalentes, con energías de disociación típicas de solo 15-25 kJ / mol, tienen una influencia significativa en las propiedades físicas de un compuesto. Los compuestos como el HF pueden formar solo dos enlaces de hidrógeno a la vez, como puede, en promedio, NH líquido puro 3 . En consecuencia, aunque sus masas moleculares son similares a las del agua, sus puntos de ebullición son significativamente más bajos que el punto de ebullición del agua, que forma cuatro enlaces de hidrógeno a la vez.
Summary
Intermolecular forces are electrostatic in nature and include van der Waals forces and hydrogen bonds. Molecules in liquids are held to other molecules by intermolecular interactions, which are weaker than the intramolecular interactions that hold the atoms together within molecules and polyatomic ions. Transitions between the solid and liquid or the liquid and gas phases are due to changes in intermolecular interactions but do not affect intramolecular interactions. The three major types of intermolecular interactions are dipole–dipole interactions, London dispersion forces (these two are often referred to collectively as van der Waals forces ), and hydrogen bonds. Dipole–dipole interactions arise from the electrostatic interactions of the positive and negative ends of molecules with permanent dipole moments; their strength is proportional to the magnitude of the dipole moment and to 1/ r 3 , where r is the distance between dipoles. London dispersion forces are due to the formation of instantaneous dipole moments in polar or nonpolar molecules as a result of short-lived fluctuations of electron charge distribution, which in turn cause the temporary formation of an induced dipole in adjacent molecules. their energy falls off as 1/ r 6 . Larger atoms tend to be more polarizable than smaller ones because their outer electrons are less tightly bound and are therefore more easily perturbed. Hydrogen bonds are especially strong dipole–dipole interactions between molecules that have hydrogen bonded to a highly electronegative atom, such as O, N, or F. The resulting partially positively charged H atom on one molecule (the hydrogen bond donor ) can interact strongly with a lone pair of electrons of a partially negatively charged O, N, or F atom on adjacent molecules (the hydrogen bond acceptor ). Because of strong O⋅⋅⋅H hydrogen bonding between water molecules, water has an unusually high boiling point, and ice has an open, cagelike structure that is less dense than liquid water.