Experimentalmente se encuentra que la solubilidad de la mayoría de los compuestos depende en gran medida de la temperatura y, si es un gas, también de la presión. Como veremos, la capacidad de manipular la solubilidad cambiando la temperatura y la presión tiene varias consecuencias importantes.
Efecto de la temperatura sobre la solubilidad de los sólidos
La Figura ( PageIndex {1} ) muestra gráficos de las solubilidades de varios compuestos orgánicos e inorgánicos en agua en función de la temperatura. Aunque la solubilidad de un sólido generalmente aumenta con el aumento de la temperatura, no existe una relación simple entre la estructura de una sustancia y la dependencia de la temperatura de su solubilidad. Muchos compuestos (como la glucosa y (CH_3CO_2Na )) exhiben un aumento dramático en la solubilidad al aumentar la temperatura. Otros (como (NaCl ) y (K_2SO_4 )) exhiben poca variación, y aún otros (como (Li_2SO_4 )) se vuelven menos solubles con el aumento de la temperatura.
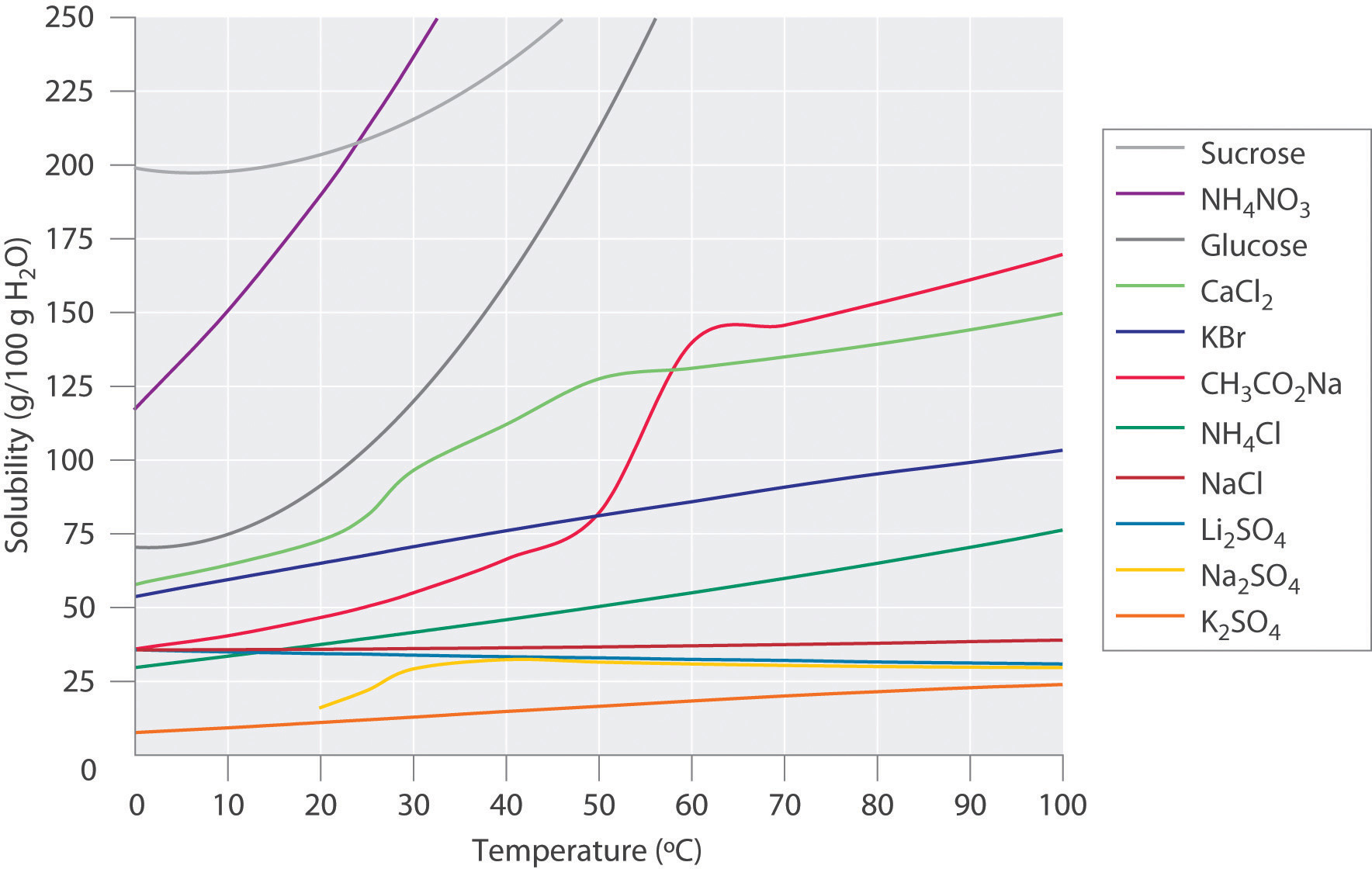
Observe en particular las curvas para (NH_4NO_3 ) y (CaCl_2 ). La disolución del nitrato de amonio en el agua es endotérmica ( (ΔH_ {soln} = +25.7 ; kJ / mol )), mientras que la disolución del cloruro de calcio es exotérmica ( (ΔH_ {soln} = −68.2 ; kJ / mol )), pero la Figura ( PageIndex {1} ) muestra que la solubilidad de ambos compuestos aumenta bruscamente con el aumento de la temperatura. De hecho, las magnitudes de los cambios tanto en la entalpía como en la entropía para la disolución dependen de la temperatura. Debido a que la solubilidad de un compuesto está determinada en última instancia por diferencias relativamente pequeñas entre números grandes, generalmente no hay una buena manera de predecir cómo la solubilidad variará con la temperatura.
La variación de la solubilidad con la temperatura se ha medido para una amplia gama de compuestos, y los resultados se publican en muchos libros de referencia estándar. Los químicos a menudo pueden usar esta información para separar los componentes de una mezcla mediante cristalización fraccionada , la separación de compuestos en función de sus solubilidades en un disolvente dado. Por ejemplo, si tenemos una mezcla de 150 g de acetato de sodio ( (CH_3CO_2Na )) y 50 g de (KBr ), podemos separar los dos compuestos disolviendo la mezcla en 100 g de agua a 80 ° C y luego enfriando la solución lentamente a 0 ° C. De acuerdo con las curvas de temperatura en la Figura ( PageIndex {1} ), ambos compuestos se disuelven en agua a 80 ° C, y los 50 g de (KBr ) permanecen en solución a 0 ° C. Sin embargo, solo alrededor de 36 g de (CH_3CO_2Na ) son solubles en 100 g de agua a 0 ° C, por lo que aproximadamente 114 g (150 g – 36 g) de (CH_3CO_2Na ) se cristalizan al enfriarse. Los cristales se pueden separar por filtración. Por lo tanto, la cristalización fraccionada nos permite recuperar aproximadamente el 75% de la (CH_3CO_2Na ) original en forma esencialmente pura en un solo paso.
La cristalización fraccionada es una técnica común para purificar compuestos tan diversos como los mostrados en la Figura ( PageIndex {1} ) y desde antibióticos hasta enzimas. Para que la técnica funcione correctamente, el compuesto de interés debe ser más soluble a alta temperatura que a baja temperatura, de modo que al bajar la temperatura se cristalice en la solución. Además, las impurezas deben ser más solubles que el compuesto de interés (como era (KBr ) en este ejemplo) y preferiblemente estar presentes en cantidades relativamente pequeñas.
Efecto de la temperatura sobre la solubilidad de los gases
La solubilidad de los gases en líquidos disminuye con el aumento de la temperatura, como se muestra en la Figura ( PageIndex {2} ). Las interacciones intermoleculares atractivas en la fase gaseosa son esencialmente cero para la mayoría de las sustancias. Cuando un gas se disuelve, lo hace porque sus moléculas interactúan con moléculas solventes. Debido a que se libera calor cuando se forman estas nuevas interacciones atractivas, la disolución de la mayoría de los gases en líquidos es un proceso exotérmico ( (ΔH_ {soln} <0 )). Por el contrario, agregar calor a la solución proporciona energía térmica que supera las fuerzas de atracción entre el gas y las moléculas del solvente, disminuyendo así la solubilidad del gas. El fenómeno es similar al involucrado en el aumento de la presión de vapor de un líquido puro con el aumento de la temperatura. En el caso de la presión de vapor, sin embargo, las fuerzas atractivas entre las moléculas de solvente son superadas por la energía térmica agregada cuando aumenta la temperatura.
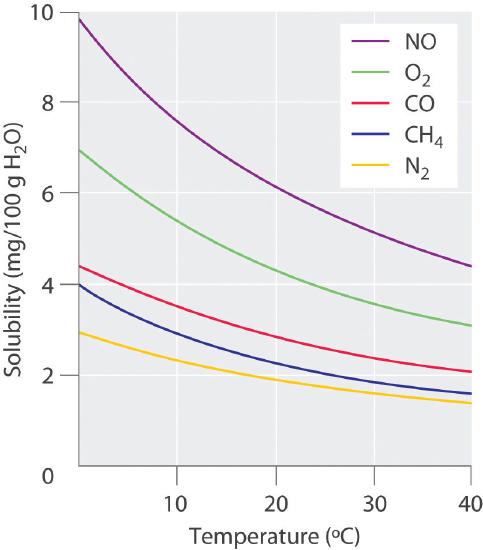
La disminución de la solubilidad de los gases a temperaturas más altas tiene implicaciones prácticas y ambientales. Cualquiera que rutinariamente hierva agua en una tetera o hervidor de agua eléctrico sabe que se acumula un depósito blanco o gris en el interior y que finalmente debe eliminarse. El mismo fenómeno ocurre a una escala mucho mayor en las calderas gigantes utilizadas para suministrar agua caliente o vapor para aplicaciones industriales, donde se llama “escala de caldera”, un depósito que puede disminuir seriamente la capacidad de las tuberías de agua caliente (Figura ( Índice de página {3} )). El problema no es único y moderno: los acueductos que fueron construidos por los romanos hace 2000 años para transportar agua fría de las regiones alpinas a regiones más cálidas y secas del sur de Francia estaban obstruidos por depósitos similares. La química detrás de la formación de estos depósitos es moderadamente compleja y se describirá en otra parte, pero la fuerza impulsora es la pérdida de (CO_2 ) disuelto de la solución. El agua dura contiene iones (Ca ^ {2 +} ) y (HCO_3 ^ – ) (bicarbonato) disueltos. El bicarbonato de calcio ( (Ca (HCO_3) _2 ) es bastante soluble en agua, pero el carbonato de calcio ( (CaCO_3 )) es bastante insoluble. Una solución de iones de bicarbonato puede reaccionar para formar dióxido de carbono, ion carbonato y agua:
[2HCO ^ -_ {3 (aq)} rightarrow CO ^ {2 -} _ {3 (aq)} + H_2O _ {(l)} + CO_ {2 (aq)} label {13.9} ]
El calentamiento de la solución disminuye la solubilidad de (CO_2 ), que escapa a la fase gaseosa por encima de la solución. En presencia de iones de calcio, los iones de carbonato precipitan como carbonato de calcio insoluble, el componente principal de la escala de la caldera.


En la contaminación térmica, el agua del lago o río que se usa para enfriar un reactor industrial o una planta de energía se devuelve al medio ambiente a una temperatura más alta de lo normal. Debido a la solubilidad reducida de (O_2 ) a temperaturas más altas (Figura ( PageIndex {2} )), el agua más cálida contiene menos oxígeno disuelto que el agua cuando entró en la planta. Los peces y otros organismos acuáticos que necesitan oxígeno disuelto para vivir pueden literalmente asfixiarse si la concentración de oxígeno de su hábitat es demasiado baja. Debido a que el agua tibia y empobrecida en oxígeno es menos densa, tiende a flotar sobre el agua más fría, más densa y más rica en oxígeno en el lago o río, formando una barrera que evita que el oxígeno atmosférico se disuelva. Eventualmente, incluso los lagos profundos pueden asfixiarse si el problema no se corrige. Además, la mayoría de los peces y otros organismos acuáticos no mamíferos son de sangre fría, lo que significa que su temperatura corporal es la misma que la temperatura de su entorno. Las temperaturas sustancialmente mayores que el rango normal pueden provocar estrés severo o incluso la muerte. Los sistemas de enfriamiento para plantas de energía y otras instalaciones deben estar diseñados para minimizar cualquier efecto adverso sobre las temperaturas de los cuerpos de agua circundantes.
Se observa un efecto similar en el aumento de las temperaturas de los cuerpos de agua como la Bahía de Chesapeake, el estuario más grande de América del Norte, donde el calentamiento global ha sido implicado como la causa. Por cada 1.5 ° C que el agua de la bahía se calienta, la capacidad del agua para disolver oxígeno disminuye en aproximadamente 1.1%. Muchas especies marinas que se encuentran en el límite sur de sus distribuciones han desplazado sus poblaciones más al norte. En 2005, la hierba de anguila, que forma un importante hábitat de vivero para peces y mariscos, desapareció de gran parte de la bahía tras las altas temperaturas récord del agua. Presumiblemente, la disminución de los niveles de oxígeno disminuyó las poblaciones de almejas y otros alimentadores de filtro, lo que luego disminuyó la transmisión de luz para permitir que crezca la hierba de anguila. Las complejas relaciones en ecosistemas como la Bahía de Chesapeake son especialmente sensibles a las fluctuaciones de temperatura que causan un deterioro de la calidad del hábitat.
Efecto de la presión sobre la solubilidad de los gases: Ley de Henry
La presión externa tiene muy poco efecto sobre la solubilidad de líquidos y sólidos. Por el contrario, la solubilidad de los gases aumenta a medida que aumenta la presión parcial del gas por encima de una solución. Este punto se ilustra en la Figura ( PageIndex {4} ), que muestra el efecto del aumento de la presión sobre el equilibrio dinámico que se establece entre las moléculas de gas disuelto en solución y las moléculas en la fase gaseosa por encima de la solución. Debido a que la concentración de moléculas en la fase gaseosa aumenta al aumentar la presión, la concentración de moléculas de gas disuelto en la solución en equilibrio también es mayor a presiones más altas.
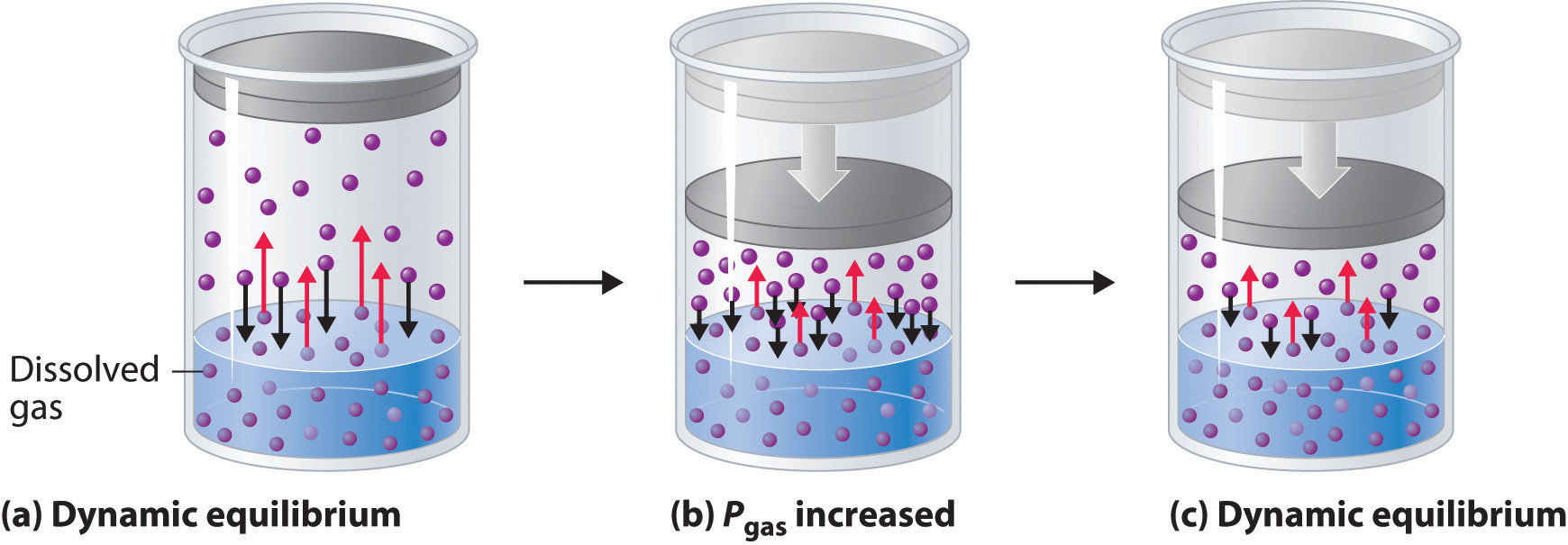
La relación entre la presión y la solubilidad de un gas se describe cuantitativamente por la ley de Henry, que lleva el nombre de su descubridor, el médico y químico inglés William Henry (1775-1836):
[C = kP label {13.3.1} ]
donde
- (C ) es la concentración de gas disuelto en equilibrio,
- (P ) es la presión parcial del gas, y
- (k ) es la constante de la ley de Henry, que debe determinarse experimentalmente para cada combinación de gas, disolvente y temperatura.
Aunque la concentración de gas puede expresarse en cualquier unidad conveniente, utilizaremos exclusivamente la molaridad. Las unidades de la constante de la ley de Henry son, por lo tanto, mol / (L · atm) = M / atm. Los valores de las constantes de la ley de Henry para soluciones de varios gases en agua a 20 ° C se enumeran en la Tabla ( PageIndex {1} ).
Como demuestran los datos de la Tabla ( PageIndex {1} ), la concentración de un gas disuelto en agua a una presión dada depende en gran medida de sus propiedades físicas. Para una serie de sustancias relacionadas, las fuerzas de dispersión de Londres aumentan a medida que aumenta la masa molecular. Así, entre los elementos del grupo 18 , las constantes de la ley de Henry aumentan sin problemas de He a Ne a Ar. La tabla también muestra que (O_2 ) es casi el doble de soluble que (N_2 ). Aunque las fuerzas de dispersión de Londres son demasiado débiles para explicar una diferencia tan grande, (O_2 ) es paramagnético y, por lo tanto, más polarizable que (N_2 ), lo que explica su alta solubilidad.
| Gas | Constante de la ley de Henry [mol / (L · atm)] × 10 −4 |
|---|---|
| (Él ) | 3,9 |
| (Ne ) | 4,7 |
| (Ar ) | 15 |
| (H_2 ) | 8.1 |
| (N_2 ) | 7.1 |
| (O_2 ) | 14 |
| (CO_2 ) | 392 |
Los gases que reaccionan químicamente con agua, como (HCl ) y los otros haluros de hidrógeno, (H_2S ) y (NH_3 ), no obedecen la ley de Henry; Todos estos gases son mucho más solubles de lo previsto por la ley de Henry. Por ejemplo, (HCl ) reacciona con agua para dar moléculas (H ^ + _ {(aq)} ) y (Cl ^ -_ {(aq)} ), no disueltas (HCl ), y su disociación en iones resulta en una solubilidad mucho mayor de lo esperado para una molécula neutra.
Los gases que reaccionan con agua no obedecen la ley de Henry.
La ley de Henry tiene aplicaciones importantes. Por ejemplo, se forman burbujas de (CO_2 ) tan pronto como se abre una bebida carbonatada porque la bebida se embotelló bajo (CO_2 ) a una presión superior a 1 atm. Cuando se abre la botella, la presión de (CO_2 ) sobre la solución cae rápidamente, y parte del gas disuelto escapa de la solución en forma de burbujas. La ley de Henry también explica por qué los buzos deben tener cuidado de ascender lentamente a la superficie después de una inmersión si respiran aire comprimido. A las presiones más altas bajo el agua, se disuelve más N2 del aire en los fluidos internos del buzo. Si el buzo asciende demasiado rápido, el cambio rápido de presión hace que se formen pequeñas burbujas de N2 en todo el cuerpo, una condición conocida como “las curvas”. Estas burbujas pueden bloquear el flujo de sangre a través de los pequeños vasos sanguíneos, causando un gran dolor e incluso resultando fatal en algunos casos.
Debido a la baja constante de la ley de Henry para (O_2 ) en el agua, los niveles de oxígeno disuelto en el agua son demasiado bajos para satisfacer las necesidades energéticas de los organismos multicelulares, incluidos los humanos. Para aumentar la concentración de (O_2 ) en los fluidos internos, los organismos sintetizan moléculas transportadoras altamente solubles que se unen a (O_2 ) de forma reversible. Por ejemplo, los glóbulos rojos humanos contienen una proteína llamada hemoglobina que se une específicamente a (O_2 ) y facilita su transporte desde los pulmones a los tejidos, donde se usa para oxidar las moléculas de los alimentos para proporcionar energía. La concentración de hemoglobina en la sangre normal es de aproximadamente 2.2 mM, y cada molécula de hemoglobina puede unir cuatro (O_2 ) moléculas. Aunque la concentración de (O_2 ) disuelto en el suero sanguíneo a 37 ° C (temperatura corporal normal) es de solo 0.010 mM, la concentración total de (O_2 ) disuelta es de 8.8 mM, casi mil veces mayor de lo que sería posible sin hemoglobina. Los portadores de oxígeno sintético basados en alcanos fluorados se han desarrollado para su uso como reemplazo de emergencia para la sangre completa. A diferencia de la sangre donada, estos “sustitutos de la sangre” no requieren refrigeración y tienen una larga vida útil. Sus constantes de ley de Henry muy altas para (O_2 ) dan como resultado concentraciones de oxígeno disuelto comparables a las de la sangre normal.
Resumen
La solubilidad de la mayoría de las sustancias depende en gran medida de la temperatura y, en el caso de los gases, de la presión. La solubilidad de la mayoría de los solutos sólidos o líquidos aumenta con el aumento de la temperatura. Los componentes de una mezcla a menudo se pueden separar mediante cristalización fraccionada, que separa los compuestos de acuerdo con sus solubilidades. La solubilidad de un gas disminuye al aumentar la temperatura. La ley de Henry describe la relación entre la presión y la solubilidad de un gas.