Una reacción de neutralización puede definirse como la reacción de un ácido y una base para producir una sal y agua. Es decir, otro catión, como (Na ^ + ), reemplaza al protón en el ácido. Un ejemplo es la reacción de (CH_3CO_2H ), un ácido débil, con (NaOH ), una base fuerte:
[ underset {acid} {CH_3CO_2H _ {(l)}} + underset {base} {NaOH _ {(s)}} overset {H_2O} { longrightarrow} underset {salt} {H_2OCH_3CO_2Na _ {( aq)}} + underset {agua} {H_2O _ {(l)}} ]
Dependiendo de las propiedades ácido-base de sus iones componentes, sin embargo, una sal puede disolverse en agua para producir una solución neutra, una solución básica o una solución ácida.
Cuando una sal como (NaCl ) se disuelve en agua, produce iones (Na ^ + _ {(aq)} ) y (Cl ^ −_ {(aq)} ). Usando un enfoque de Lewis, el ion (Na ^ + ) puede verse como un ácido porque es un receptor de pares de electrones, aunque su baja carga y su radio relativamente grande lo convierten en un ácido muy débil. El ion (Cl ^ – ) es la base conjugada del ácido fuerte (HCl ), por lo que esencialmente no tiene un carácter básico. En consecuencia, la disolución de (NaCl ) en agua no tiene efecto sobre el (pH ) de una solución, y la solución permanece neutral.
Ahora comparemos este comportamiento con el comportamiento de las soluciones acuosas de cianuro de potasio y acetato de sodio. Nuevamente, los cationes ( (K ^ + ) y (Na ^ + )) esencialmente no tienen carácter ácido, pero los aniones ( (CN ^ – ) y (CH_3CO_2 ^ – )) son bases débiles que pueden reaccionar con el agua porque son las bases conjugadas de los ácidos débiles (HCN ) y el ácido acético, respectivamente.
[CN ^ -_ {(aq)} + H_2O _ {(l)} ce {<< =>} HCN _ {(aq)} + OH ^ -_ {(aq)} ]
[CH_3CO ^ 2_ {2 (aq)} + H_2O _ {(l)} ce {<< =>} CH_3CO_2H _ {(aq)} + OH ^ -_ {(aq)} ]
Ninguna de las reacciones avanza muy a la derecha como está escrita porque se favorece la formación del par ácido-base más débil. Tanto (HCN ) como el ácido acético son ácidos más fuertes que el agua, y el hidróxido es una base más fuerte que el acetato o el cianuro, por lo que en ambos casos, el equilibrio se encuentra a la izquierda. Sin embargo, cada una de estas reacciones genera suficientes iones de hidróxido para producir una solución básica. Por ejemplo, el (pH ) de una solución 0.1 M de acetato de sodio o cianuro de potasio a 25 ° C es 8.8 u 11.1, respectivamente. De la Tabla ( PageIndex {1} ) y la Figura ( PageIndex {1} ), podemos ver que (CN ^ – ) es una base más fuerte ( (pK_b = 4.79 )) que el acetato ( (pK_b = 9.24 )), que es consistente con (KCN ) que produce una solución más básica que el acetato de sodio a la misma concentración.
En contraste, el ácido conjugado de una base débil debe ser un ácido débil (Ecuación ( ref {16.2} )). Por ejemplo, el cloruro de amonio y el cloruro de piridinio son sales producidas por reacción de amoníaco y piridina, respectivamente, con (HCl ). Como ya sabe, el ion cloruro es una base tan débil que no reacciona con el agua. En contraste, los cationes de las dos sales son ácidos débiles que reaccionan con el agua de la siguiente manera:
[NH ^ + _ {4 (aq)} + H_2O _ {(l)} ce {<< =>} HH_ {3 (aq)} + H_3O ^ + _ {(aq)} label { 16.2} ]
[C_5H_5NH ^ + _ {(aq)} + H_2O _ {(l)} ce {<< =>} C_5H_5NH _ {(aq)} + H_3O ^ + _ {(aq)} label {16.3} ]
La ecuación ( ref {16.2} ) indica que (H_3O ^ + ) es un ácido más fuerte que (NH_4 ^ + ) o (C_5H_5NH ^ + ), y por el contrario, amoníaco y piridina son ambas bases más fuertes que el agua. Por lo tanto, el equilibrio estará muy a la izquierda en ambos casos, favoreciendo el par ácido-base más débil. Sin embargo, la concentración de (H_3O ^ + ) producida por las reacciones es lo suficientemente grande como para disminuir significativamente el (pH ) de la solución: el (pH ) de una solución 0,10 M de cloruro de amonio o cloruro de piridinio a 25 ° C es 5.13 o 3.12, respectivamente. Esto es consistente con la información que se muestra en la Figura 16.2, lo que indica que el ion piridinio es más ácido que el ion amonio.
¿Qué sucede con las soluciones acuosas de una sal como el acetato de amonio, donde tanto el catión como el anión pueden reaccionar por separado con agua para producir un ácido y una base, respectivamente? De acuerdo con la Figura 16.10, el ion amonio reducirá el (pH ), mientras que de acuerdo con la Ecuación ( ref {16.3} ), el ion acetato elevará el (pH ). Este caso particular es inusual, ya que el catión es un ácido tan fuerte como el anión es una base (pKa ≈ pKb). En consecuencia, los dos efectos se cancelan y la solución permanece neutral. Con sales en las que el catión es un ácido más fuerte que el anión como base, la solución final tiene un (pH ) <7.00. Por el contrario, si el catión es un ácido más débil que el anión es una base, la solución final tiene un (pH )> 7.00.
Las soluciones de sales simples de iones metálicos también pueden ser ácidas, aunque un ion metálico no puede donar un protón directamente al agua para producir (H_3O ^ + ). En cambio, un ion metálico puede actuar como un ácido de Lewis e interactuar con el agua, una base de Lewis, coordinando un par solitario de electrones en el átomo de oxígeno para formar un ion metálico hidratado (parte (a) en la Figura ( PageIndex { 1} )). Una molécula de agua coordinada a un ion metálico es más ácida que una molécula de agua libre por dos razones. Primero, las interacciones electrostáticas repulsivas entre el ion metálico cargado positivamente y los átomos de hidrógeno parcialmente cargados positivamente de la molécula de agua coordinada facilitan que el agua coordinada pierda un protón.
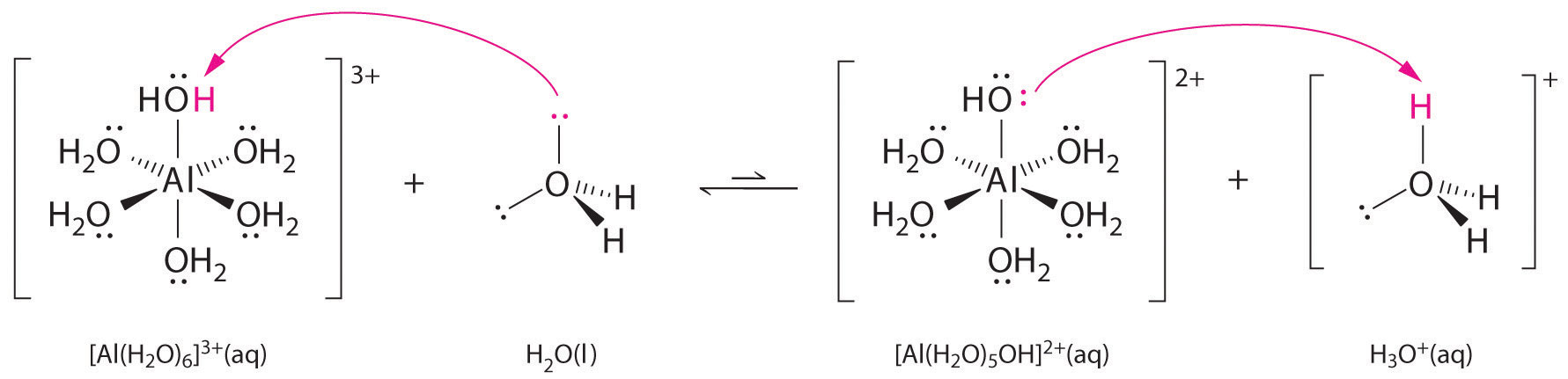
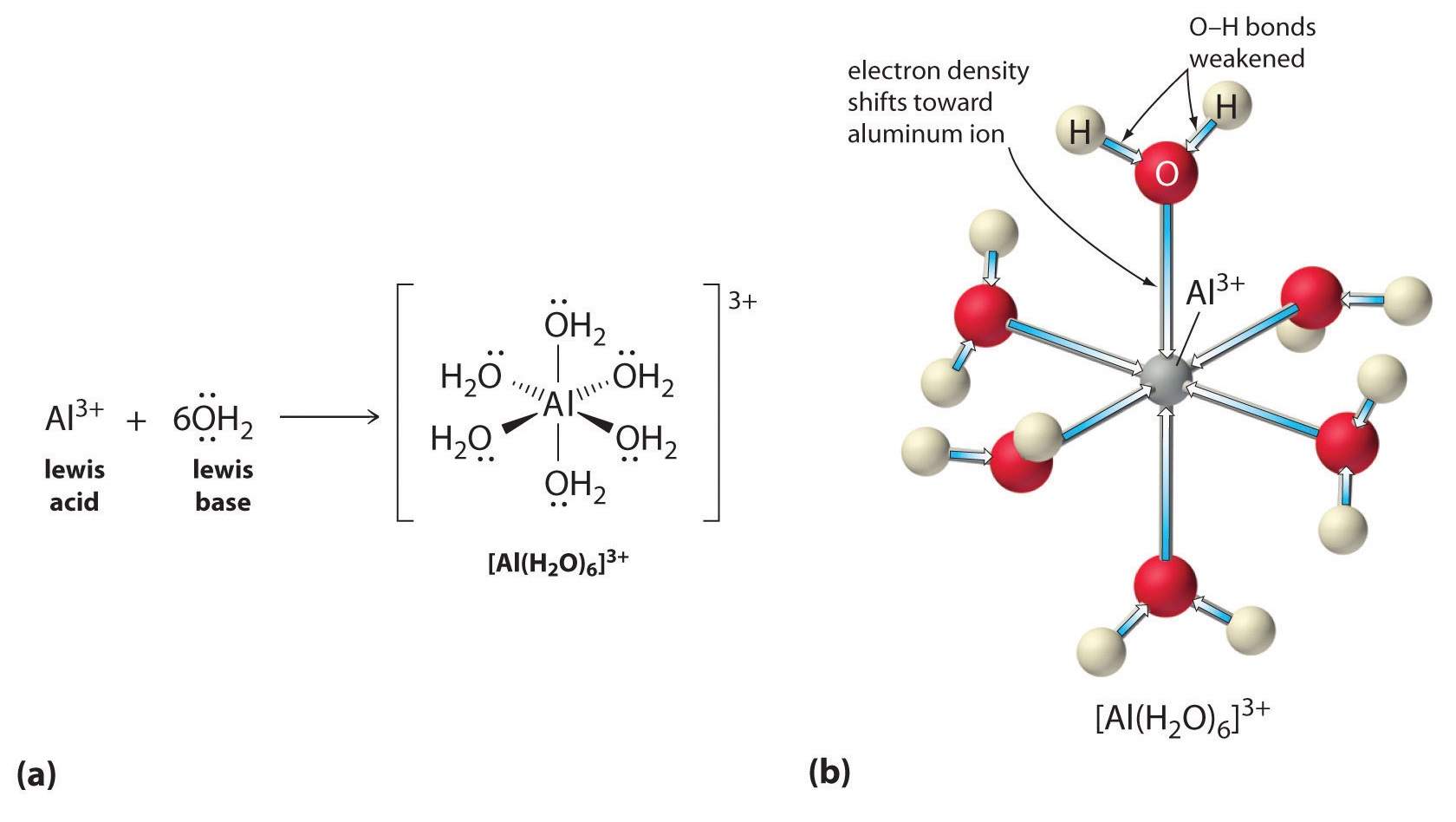
La magnitud de este efecto depende de los siguientes dos factores (Figura ( PageIndex {2} )):
- La carga en el ion metálico. Un ion divalente ( (M ^ {2 +} )) tiene un efecto aproximadamente dos veces mayor en la densidad de electrones en una molécula de agua coordinada que un ion monovalente ( (M ^ + )) del mismo radio.
- El radio del ion metálico. Para los iones metálicos con la misma carga, cuanto más pequeño es el ión, más corta es la distancia internuclear al átomo de oxígeno de la molécula de agua y mayor es el efecto del metal sobre la distribución de densidad electrónica en la molécula de agua.
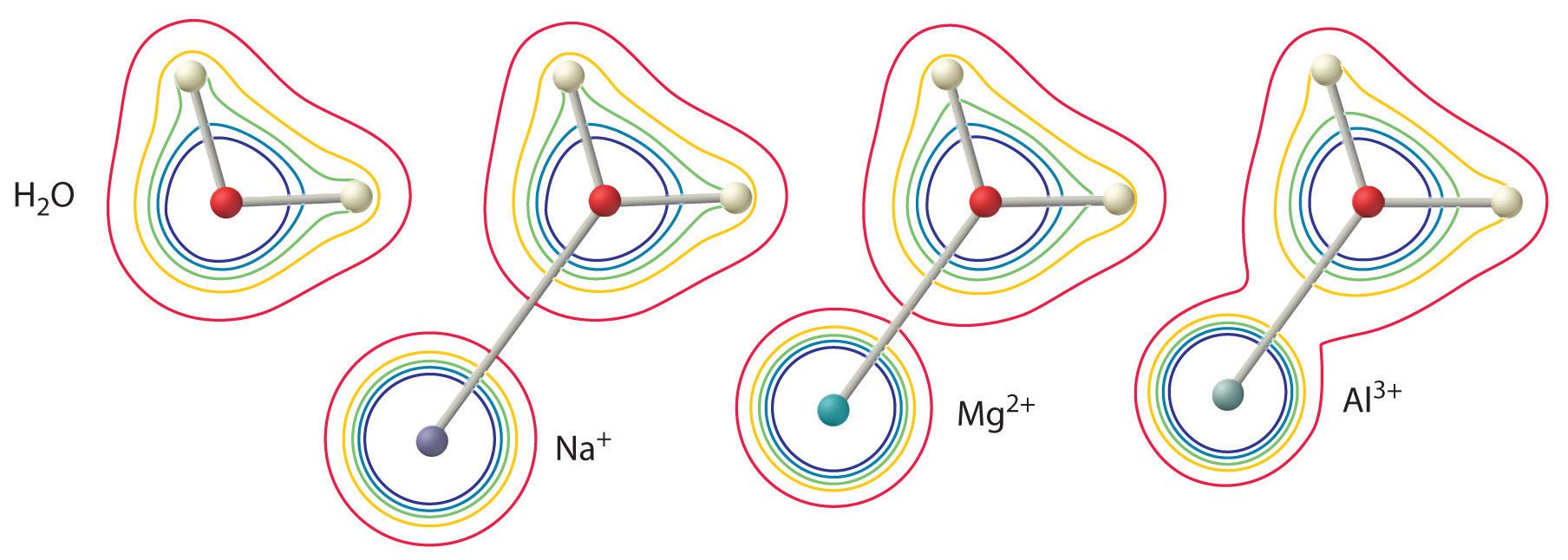
Por lo tanto, las soluciones acuosas de iones metálicos pequeños y altamente cargados, como (Al ^ {3 +} ) y (Fe ^ {3 +} ), son ácidos:
[[Al (H_2O) _6] ^ {3 +} _ {(aq)} rightleftharpoons [Al (H_2O) _5 (OH)] ^ {2 +} _ {(aq)} + H ^ + _ {(aq)} label {16.36} ]
El ion ([Al (H_2O) _6] ^ {3 +} ) tiene un (pK_a ) de 5.0, lo que lo convierte en un ácido casi tan fuerte como el ácido acético. Debido a los dos factores descritos anteriormente, el parámetro más importante para predecir el efecto de un ion metálico sobre la acidez de las moléculas de agua coordinadas es la relación carga-radio del ion metálico. Una serie de pares de iones metálicos que se encuentran en una línea diagonal en la tabla periódica, como (Li ^ + ) y (Mg ^ {2 +} ) o (Ca ^ {2 +} ) y (Y ^ {3 +} ), tienen diferentes tamaños y cargas, pero proporciones similares de carga a radio. Como resultado, estos pares de iones metálicos tienen efectos similares sobre la acidez de las moléculas de agua coordinadas, y a menudo exhiben también otras similitudes significativas en química.
Las soluciones de iones metálicos pequeños y altamente cargados en agua son ácidas.
Las reacciones como las discutidas en esta sección, en las que una sal reacciona con agua para dar una solución ácida o básica, a menudo se denominan reacciones de hidrólisis. El uso de un nombre diferente para este tipo de reacción es lamentable porque sugiere que de alguna manera son diferentes. De hecho, las reacciones de hidrólisis son solo reacciones ácido-base en las que el ácido es un catión o la base es un anión; obedecen los mismos principios y reglas que todas las demás reacciones ácido-base.
Una reacción de hidrólisis es una reacción ácido-base.
Resumen
Una sal puede disolverse en agua para producir una solución neutra, básica o ácida, dependiendo de si contiene la base conjugada de un ácido débil como el anión ( (A ^ – )), el ácido conjugado de una base débil como el catión ( (BH ^ + )), o ambos. Las sales que contienen iones metálicos pequeños y altamente cargados producen soluciones ácidas en agua. La reacción de una sal con agua para producir una solución ácida o básica se llama reacción de hidrólisis.
Puntos clave
- Las reacciones ácido-base siempre contienen dos pares conjugados de ácido-base.
- Cada ácido y cada base tiene una constante de ionización asociada que corresponde a su ácido o fuerza base.