Al comenzar nuestro resumen de tendencias periódicas, recordemos que el principio unificador más importante para comprender la química de los elementos es el aumento sistemático del número atómico, acompañado del llenado ordenado de los orbitales atómicos por electrones, lo que conduce a la periodicidad. en propiedades tales como tamaño atómico e iónico, energía de ionización, electronegatividad y afinidad electrónica. Los mismos factores también conducen a la periodicidad en las configuraciones de electrones de valencia, lo que para cada grupo produce similitudes en los estados de oxidación y la formación de compuestos con estequiometrías comunes.
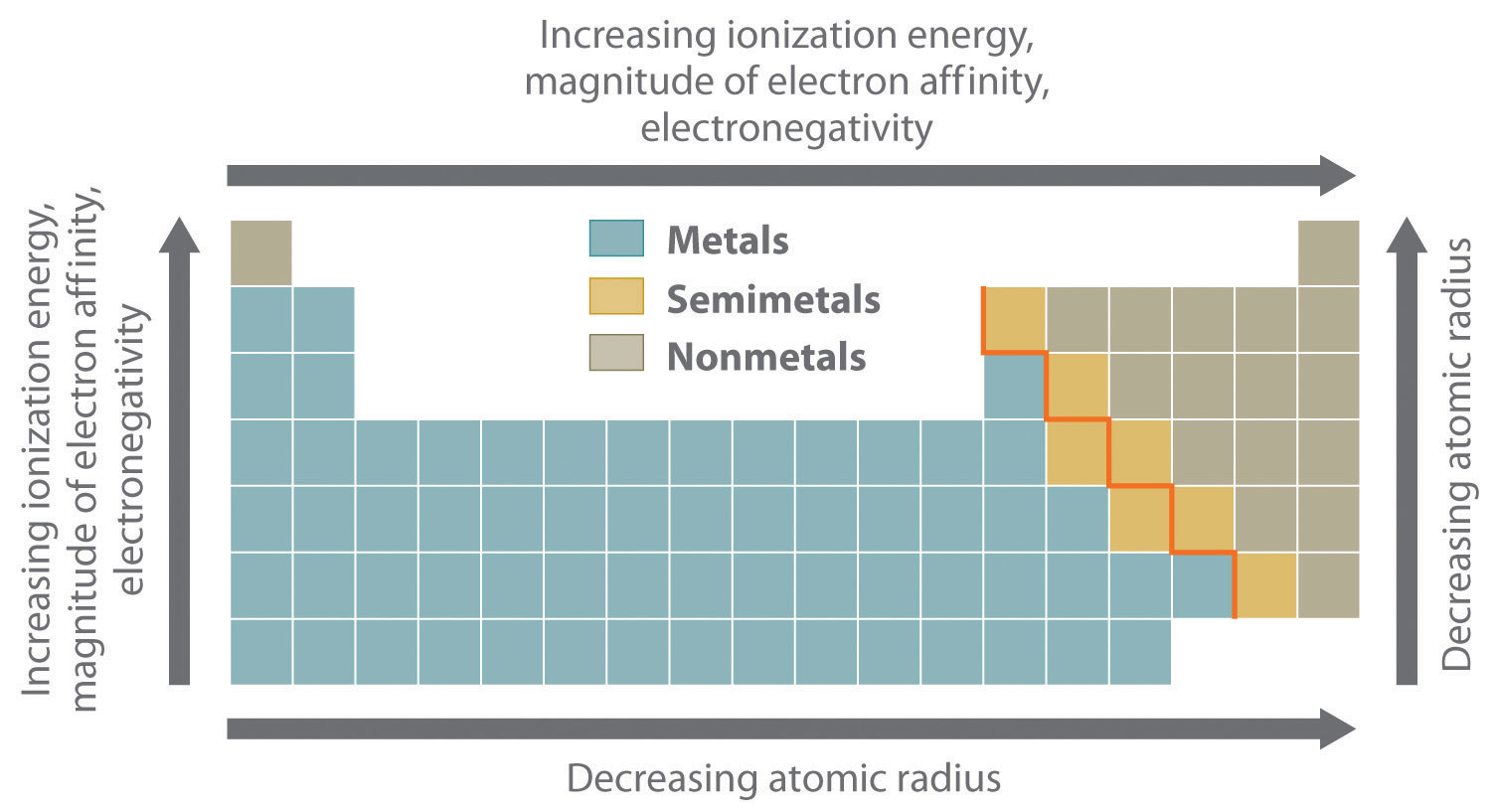
Las tendencias periódicas más importantes en las propiedades atómicas se resumen en la Figura ( PageIndex {1} ). Recuerde que estas tendencias se basan en variaciones periódicas en una sola propiedad fundamental, la carga nuclear efectiva (Z eff ), que aumenta de izquierda a derecha y de arriba a abajo en la periódica mesa.
La línea diagonal en la Figura ( PageIndex {1} ) separa los metales (a la izquierda de la línea) de los no metales (a la derecha de la línea). Debido a que los metales tienen electronegatividades relativamente bajas, tienden a perder electrones en reacciones químicas a elementos que tienen electronegatividades relativamente altas, formando compuestos en los que tienen estados de oxidación positivos. Por el contrario, los no metales tienen altas electronegatividades y, por lo tanto, tienden a ganar electrones en reacciones químicas para formar compuestos en los que tienen estados de oxidación negativos. Los semimetales se encuentran a lo largo de la línea diagonal que divide los metales y los no metales. No es sorprendente que tiendan a exhibir propiedades y reactividades intermedias entre las de los metales y los no metales. Debido a que los elementos de los grupos 13, 14 y 15 abarcan la línea diagonal que separa metales y no metales, su química es más compleja de lo previsto basándose únicamente en sus configuraciones electrónicas de valencia.
Química única de los elementos más ligeros
La química del elemento del segundo período de cada grupo (n = 2: Li, Be, B, C, N, O y F) difiere en muchos aspectos importantes de la de los miembros más pesados, o congéneres, de el grupo. En consecuencia, los elementos del tercer período (n = 3: Na, Mg, Al, Si, P, S y Cl) son generalmente más representativos del grupo al que pertenecen. La química anómala de los elementos del segundo período es el resultado de tres características importantes: radios pequeños, d orbitales energéticamente no disponibles y una tendencia a formar enlaces pi (π) con otros átomos.
En contraste con la química de los elementos del segundo período, la química de los elementos del tercer período es más representativa de la química del grupo respectivo.
Debido a su pequeño radio, los elementos del segundo período tienen afinidades electrónicas que son menos negativas de lo que se predeciría a partir de las tendencias periódicas generales. Cuando se agrega un electrón a un átomo tan pequeño, el aumento de las repulsiones electrón-electrón tiende a desestabilizar el anión. Además, los tamaños pequeños de estos elementos les impiden formar compuestos en los que tienen más de cuatro vecinos más cercanos. Así, BF 3 forma solo el ión tetraédrico de cuatro coordenadas BF 4 – , mientras que en las mismas condiciones AlF 3 forma los seis -coordinado, octaédrico AlF 6 3− ion. Debido al tamaño atómico más pequeño, los compuestos iónicos binarios simples de elementos del segundo período también tienen un carácter más covalente que los compuestos correspondientes formados a partir de sus congéneres más pesados. Los cationes muy pequeños derivados de elementos del segundo período tienen una alta relación carga-radio y, por lo tanto, pueden polarizar la capa de valencia llena de un anión. Como tal, la unión en tales compuestos tiene un componente covalente significativo, lo que proporciona a los compuestos propiedades que pueden diferir significativamente de las esperadas para los compuestos iónicos simples. Como ejemplo, el LiCl, que tiene un carácter parcialmente covalente, es mucho más soluble que el NaCl en solventes con una constante dieléctrica relativamente baja, como el etanol (ε = 25.3 versus 80.1 para H 2 O).
Debido a que los orbitales d nunca se ocupan para los números cuánticos principales menores que 3, los electrones de valencia de los elementos del segundo período ocupan solo los orbitales 2s y 2p. La energía de los orbitales 3d supera con creces la energía de los orbitales 2s y 2p, por lo que usarlos en la unión es energéticamente prohibitivo. En consecuencia, las configuraciones de electrones con más de cuatro pares de electrones alrededor de un elemento central del segundo período simplemente no se observan. Puede recordar que el papel de los d orbitales en la unión en compuestos del grupo principal con números de coordinación de 5 o más sigue siendo algo controvertido. De hecho, se han publicado descripciones teóricas de la unión en moléculas como SF 6 sin mencionar la participación de orbitales d en azufre. Sin embargo, los argumentos basados en la disponibilidad d-orbital y en el pequeño tamaño del átomo central predicen que los números de coordinación mayores que 4 son inusuales para los elementos del segundo período, lo cual está de acuerdo con los resultados experimentales.
Una de las diferencias más dramáticas entre los elementos del grupo principal más livianos y sus congéneres más pesados es la tendencia de los elementos del segundo período a formar especies que contienen enlaces múltiples. Por ejemplo, N está justo por encima de P en el grupo 15: N 2 contiene un enlace N≡N, pero cada átomo de fósforo en tetraédrico P 4 forma tres enlaces P – P. Esta diferencia de comportamiento refleja el hecho de que dentro del mismo grupo de la tabla periódica, las energías relativas del enlace π y el enlace sigma (σ) difieren. Un enlace C = C, por ejemplo, es aproximadamente un 80% más fuerte que un enlace CC. En contraste, un enlace Si = Si, con menos solapamiento p-orbital entre los orbitales de valencia de los átomos unidos debido al mayor tamaño atómico, es solo un 40% más fuerte que un enlace Si-Si. En consecuencia, los compuestos que contienen enlaces C a C múltiples y simples son comunes para el carbono, pero los compuestos que contienen solo enlaces sigma Si-Si son más energéticamente favorables para el silicio y los otros elementos del tercer período.
Otra tendencia importante a tener en cuenta en la química del grupo principal es la similitud química entre el elemento más ligero de un grupo y el elemento inmediatamente inferior y a su derecha en el siguiente grupo, un fenómeno conocido como el efecto diagonal [ 19459025] (Figura ( PageIndex {2} )) Hay, por ejemplo, similitudes significativas entre la química de Li y Mg, Be y Al, y B y Si. Tanto BeCl 2 como AlCl 3 tienen un carácter covalente sustancial, por lo que son algo solubles en solventes orgánicos no polares. En contraste, aunque Mg y Be están en el mismo grupo, MgCl 2 se comporta como un haluro iónico típico debido a la menor electronegatividad y al mayor tamaño del magnesio.
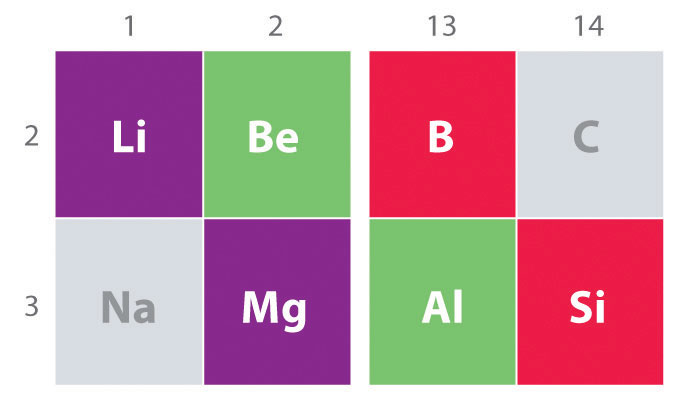
El efecto de par inerte
El efecto de par inerte se refiere a la observación empírica de que los elementos más pesados de los grupos 13-17 a menudo tienen estados de oxidación que son inferiores en 2 al máximo predicho para su grupo. Por ejemplo, aunque un estado de oxidación de +3 es común para los elementos del grupo 13, el elemento más pesado del grupo 13, el talio (Tl), es más probable que forme compuestos en los que tiene un estado de oxidación +1. Parece haber dos razones principales para el efecto del par inerte: aumentar las energías de ionización y disminuir las fuerzas de enlace.
Al descender un grupo en el bloque p, el aumento de las energías de ionización y la disminución de las fuerzas de enlace dan como resultado un efecto de par inerte.
Las energías de ionización aumentan porque las subcapas llenas (n – 1) do (n – 2) f son relativamente pobres para proteger electrones en los orbitales ns. Por lo tanto, los dos electrones en la subcapa ns experimentan una carga nuclear efectiva inusualmente alta, por lo que se sienten fuertemente atraídos por el núcleo, lo que reduce su participación en la unión. Por lo tanto, es sustancialmente más difícil de lo esperado eliminar estos electrones ns 2 , como se muestra en la Tabla ( PageIndex {1} ) por la diferencia entre las primeras energías de ionización de talio y aluminio. Debido a que Tl es menos probable que Al pierda sus dos electrones ns 2 , su estado de oxidación más común es +1 en lugar de +3.
| Elemento | Configuración electrónica | I 1 (kJ / mol) | I 1 + I 2 + I 3 (kJ / mol) | Energía media de enlace M – Cl (kJ / mol) |
|---|---|---|---|---|
| B | [Él] 2s 2 2p 1 | 801 | 6828 | 536 |
| Al | [Ne] 3s 2 3p 1 | 578 | 5139 | 494 |
| Ga | [Ar] 3d 10 4s 2 4p 1 | 579 | 5521 | 481 |
| En | [Kr] 4d 10 5s 2 p 1 | 558 | 5083 | 439 |
| Tl | [Xe] 4f 14 5d 10 6s 2 p 1 | 589 | 5439 | 373 |
Fuente de datos: John A. Dean, Lange’s Handbook of Chemistry, 15th ed. (Nueva York: McGraw-Hill, 1999).
Bajando un grupo, los átomos generalmente se hicieron más grandes, y la superposición entre los orbitales de valencia de los átomos unidos disminuye. En consecuencia, las fuerzas de unión tienden a disminuir en una columna. Como se muestra en las energías de enlace M – Cl enumeradas en la Tabla ( PageIndex {1} ), la fuerza del enlace entre un átomo del grupo 13 y un átomo de cloro disminuye en más del 30% de B a Tl. Se observan disminuciones similares para los átomos de los grupos 14 y 15.
El efecto neto de estos dos factores, el aumento de las energías de ionización y la disminución de las fuerzas de enlace, es que al descender un grupo en el bloque p, la energía adicional liberada al formar dos enlaces adicionales eventualmente no es lo suficientemente grande como para compensar el energía adicional requerida para eliminar los dos electrones ns 2 .
Ejemplo ( PageIndex {1} )
Según las posiciones de los elementos del grupo 13 en la tabla periódica y las tendencias generales descritas en esta sección,
- clasifican estos elementos como metales, semimetales o no metales.
- predice qué elemento forma los compuestos más estables en el estado de oxidación +1.
- predice qué elemento difiere más de los demás en su química.
- predice qué elemento de otro grupo exhibirá la química más similar a la de Al.
Dado: posiciones de elementos en la tabla periódica
Preguntado por: clasificación, estabilidad del estado de oxidación y reactividad química
Estrategia:
Desde la posición de la línea diagonal en la tabla periódica que separa metales y no metales, clasifique los elementos del grupo 13. Luego use las tendencias discutidas en esta sección para comparar sus estabilidades relativas y reactividades químicas.
Solución:
- El grupo 13 abarca la línea diagonal que separa los metales de los no metales. Aunque Al y B se encuentran en la línea diagonal, solo B es semimetal; Los elementos más pesados son los metales.
- Los cinco elementos en el grupo 13 tienen una ns 2 np 1 configuración de electrones de valencia, por lo que se espera que formen iones con una carga +3 por la pérdida de todos los electrones de valencia . El efecto del par inerte debería ser más importante para el elemento más pesado (Tl), por lo que es más probable que forme compuestos en un estado de oxidación que sea menor en 2. Por lo tanto, se predice que el estado de oxidación +1 es más importante para el talio.
- Entre los elementos principales del grupo, el miembro más ligero de cada grupo exhibe una química única debido a su pequeño tamaño que resulta en una alta concentración de carga, d orbitales energéticamente no disponibles y una tendencia a formar enlaces múltiples. En el grupo 13, predecimos que la química del boro será bastante diferente de la de sus congéneres más pesados.
- Dentro de los bloques syp, las similitudes entre elementos en diferentes grupos están más marcadas entre el miembro más ligero de un grupo y el elemento del siguiente grupo inmediatamente debajo ya la derecha del mismo. Estos elementos exhiben electronegatividades y relaciones de carga a radio similares. Como Al es el segundo miembro del grupo 13, predecimos que su química será más similar a la de Be, el miembro más ligero del grupo 2.
Ejercicio ( PageIndex {1} )
Basado en las posiciones del grupo 14 elementos C, Si, Ge, Sn y Pb en la tabla periódica y las tendencias generales descritas en esta sección,
- clasifican estos elementos como metales, semimetales o no metales.
- predice qué elemento forma los compuestos más estables en el estado de oxidación +2.
- predice qué elemento difiere más de los demás en su química.
- predice qué elemento del grupo 14 será químicamente más similar a un elemento del grupo 15.
Respuesta:
- no metal: C; semimetales: Si y Ge; metales: Sn y Pb
- Pb es más estable como M 2 + .
- C es muy diferente.
- C y P son más similares en química.
Resumen
La química del elemento del tercer período en un grupo es la más representativa de la química del grupo porque la química de los elementos del segundo período está dominada por sus radios pequeños, orbitales d no disponibles energéticamente y tendencia a formar enlaces π con otros átomos El principio unificador más importante al describir la química de los elementos es que el aumento sistemático del número atómico y el llenado ordenado de los orbitales atómicos conducen a tendencias periódicas en las propiedades atómicas. La propiedad más fundamental que conduce a variaciones periódicas es la carga nuclear efectiva (Z eff ). Debido a la posición de la línea diagonal que separa metales y no metales en la tabla periódica, la química de los grupos 13, 14 y 15 es relativamente compleja. Los elementos del segundo período (n = 2) en cada grupo exhiben una química única en comparación con sus congéneres más pesados debido a sus radios más pequeños, d orbitales energéticamente no disponibles y una mayor capacidad para formar enlaces π con otros átomos. El aumento de las energías de ionización y la disminución de las fuerzas de enlace conducen al efecto de par inerte, lo que hace que los elementos más pesados de los grupos 13-17 tengan un estado de oxidación estable que sea inferior en 2 al máximo previsto para sus respectivos grupos.