La afinidad electrónica ( (EA )) de un elemento (E ) se define como el cambio de energía que ocurre cuando un electrón se agrega a un átomo o ion gaseoso:
[E _ {(g)} + e ^ – rightarrow E ^ -_ {(g)} ; ; ; text {energy change =} EA label {7.5.1} ]
A diferencia de las energías de ionización, que siempre son positivas para un átomo neutro porque se requiere energía para eliminar un electrón, las afinidades electrónicas pueden ser negativas (la energía se libera cuando se agrega un electrón), positiva (se debe agregar energía al sistema producir un anión) o cero (el proceso es energéticamente neutral). Esta convención de signos es coherente con un valor negativo correspondiente al cambio de energía para un proceso exotérmico, que es uno en el que se libera calor (Figura ( PageIndex {1} )).
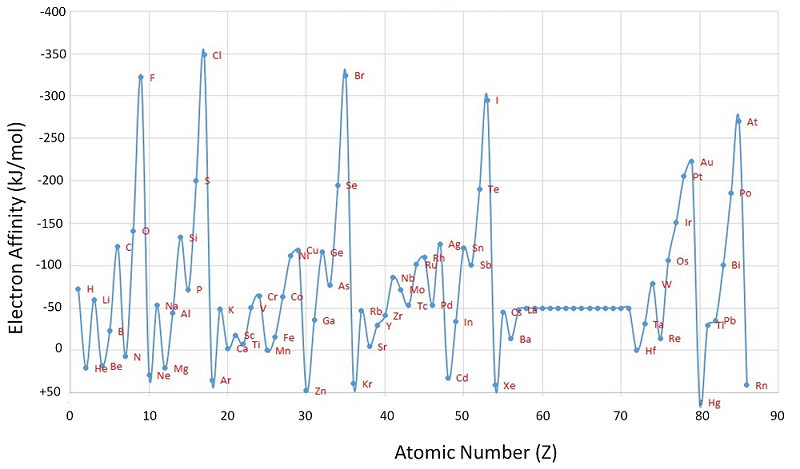
El átomo de cloro tiene la afinidad electrónica más negativa de cualquier elemento, lo que significa que se libera más energía cuando se agrega un electrón a un átomo de cloro gaseoso que a un átomo de cualquier otro elemento:
[ ce {Cl (g) + e ^ – rightarrow Cl ^ – (g)} ; ; ; EA = -346 ; kJ / mol label {7.5.2} ]
En contraste, el berilio no forma un anión estable, por lo que su afinidad electrónica efectiva es
[ ce {Be (g) + e ^ – rightarrow Be ^ – (g)} ; ; ; EA ge 0 label {7.5.3} ]
El nitrógeno es único porque tiene una afinidad electrónica de aproximadamente cero. Agregar un electrón no libera ni requiere una cantidad significativa de energía:
[ ce {N (g) + e ^ – rightarrow N ^ – (g)} ; ; ; EA aproximadamente 0 etiqueta {7.5.4} ]
Generalmente, las afinidades electrónicas se vuelven más negativas en una fila de la tabla periódica.
En general, las afinidades electrónicas de los elementos del grupo principal se vuelven menos negativas a medida que avanzamos por una columna. Esto se debe a que n aumenta, los electrones adicionales entran en los orbitales que están cada vez más lejos del núcleo.
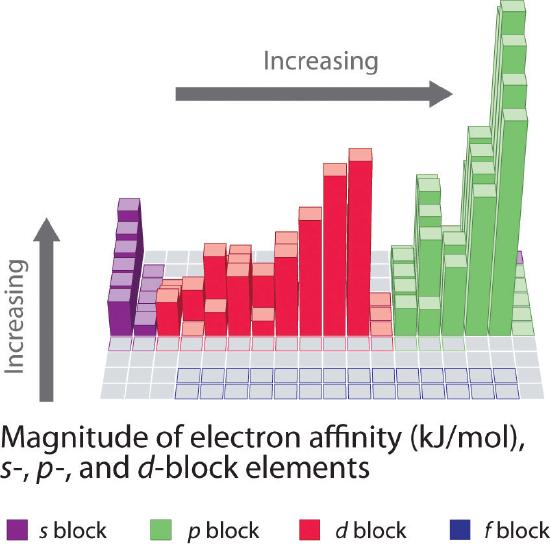
Los átomos con los radios más grandes, que tienen las energías de ionización más bajas (afinidad por sus propios electrones de valencia), también tienen la afinidad más baja por un electrón agregado. Sin embargo, hay dos grandes excepciones a esta tendencia:
- Las afinidades electrónicas de los elementos B a F en la segunda fila de la tabla periódica son menos negativas que las de los elementos inmediatamente debajo de ellas en la tercera fila. Aparentemente, el aumento de las repulsiones electrón-electrón experimentadas por los electrones confinados a los orbitales relativamente pequeños 2 p superan el aumento de la atracción electrón-núcleo a distancias nucleares cortas. El flúor, por lo tanto, tiene una menor afinidad por un electrón agregado que el cloro. En consecuencia, los elementos de la tercera fila ( n = 3) tienen las afinidades electrónicas más negativas. Más abajo en una columna, la atracción por un electrón agregado disminuye porque el electrón está entrando en un orbital más distante del núcleo. Las repulsiones electrón-electrón también disminuyen porque los electrones de valencia ocupan un mayor volumen de espacio. Estos efectos tienden a cancelarse entre sí, por lo que los cambios en la afinidad electrónica dentro de una familia son mucho más pequeños que los cambios en la energía de ionización.
- Las afinidades electrónicas de los metales alcalinotérreos se vuelven más negativas de Be a Ba. La separación de energía entre las subcapas ns 2 y las subcapas np llenas disminuye al aumentar n , de modo que la formación de un anión a partir del Los elementos más pesados se vuelven energéticamente más favorables.
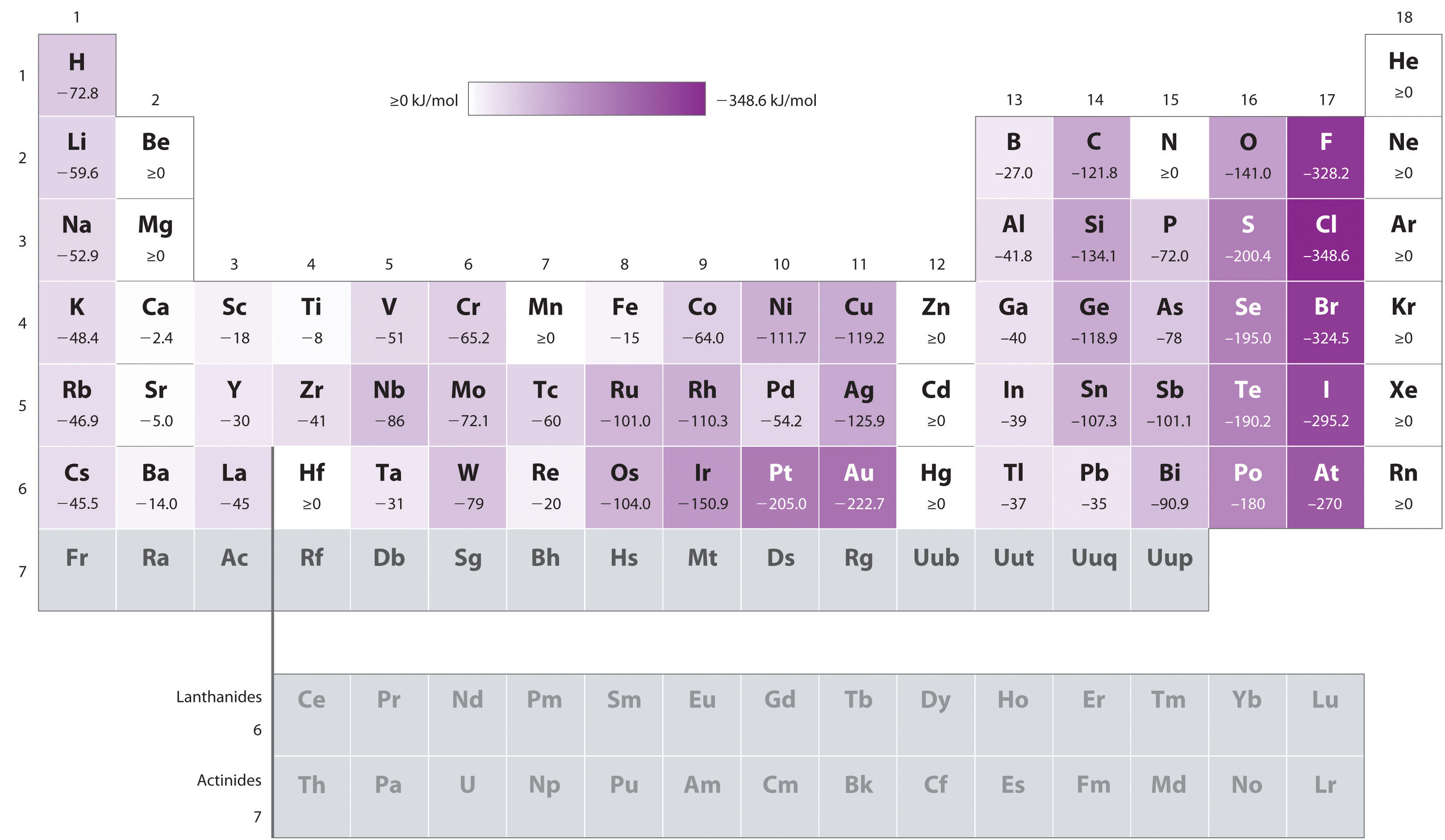
Las ecuaciones para las segundas y mayores afinidades electrónicas son análogas a las de las segundas y más altas energías de ionización:
[E _ {(g)} + e ^ – rightarrow E ^ -_ {(g)} ; ; ; text {energy change =} EA_1 label {7.5.5} ]
[E ^ -_ {(g)} + e ^ – rightarrow E ^ {2 -} _ {(g)} ; ; ; text {energy change =} EA_2 label {7.5.6} ]
Como hemos visto, la primera afinidad electrónica puede ser mayor o igual a cero o negativa, dependiendo de la configuración electrónica del átomo. En contraste, la segunda afinidad electrónica es siempre positiva porque el aumento de las repulsiones electrón-electrón en un dianión es mucho mayor que la atracción del núcleo por los electrones adicionales. Por ejemplo, la primera afinidad electrónica de oxígeno es −141 kJ / mol, pero la segunda afinidad electrónica es de +744 kJ / mol:
[O _ {(g)} + e ^ – rightarrow O ^ -_ {(g)} ; ; ; EA_1 = -141 ; kJ / mol label {7.5.7} ]
[O ^ -_ {(g)} + e ^ – rightarrow O ^ {2 -} _ {(g)} ; ; ; EA_2 = + 744 ; kJ / mol label {7.5.8} ]
Por lo tanto, la formación de un ion de óxido gaseoso ( (O ^ {2 -} )) es energéticamente bastante desfavorable (estimado mediante la adición de ambos pasos):
[O _ {(g)} + 2e ^ – rightarrow O ^ {2 -} _ {(g)} ; ; ; EA = + 603 ; kJ / mol label {7.5.9} ]
Del mismo modo, la formación de todos los dianiones comunes (como (S ^ {2 -} )) o trianiones (como (P ^ {3 -} )) es energéticamente desfavorable en la fase gaseosa.
Mientras que las afinidades del primer electrón pueden ser negativas, positivas o cero, las afinidades del segundo electrón siempre son positivas.
Si se requiere energía para formar cationes cargados positivamente y polianiones monoatómicos, ¿por qué se forman compuestos iónicos como (MgO ), (Na_2S ) y (Na_3P )? El factor clave en la formación de compuestos iónicos estables son las interacciones electrostáticas favorables entre los cationes y los aniones en la sal cristalina .
Resumen
La afinidad electrónica ( EA ) ] de un elemento es el cambio de energía que ocurre cuando un electrón se agrega a un átomo gaseoso para dar un anión. En general, los elementos con las afinidades electrónicas más negativas (la mayor afinidad por un electrón agregado) son aquellos con el tamaño más pequeño y las energías de ionización más altas y se encuentran en la esquina superior derecha de la tabla periódica.